Publié le 16 déc 2007Lecture 11 min
Cicatrisation des plaies chroniques et des brûlures : techniques spécialisées et voies de recherche
S. CAIREY-REMONNAY Centre de Traitement Ambulatoire des Plaies Chroniques, Service de dermatologie, CHU de Besançon
Nous abordons ici les techniques réservées aux cas difficiles comme les brûlures et les plaies chroniques. Certaines sont connues depuis longtemps, comme la thérapie par pression négative, mais connaissent un nouvel essort ; d’autres, comme les thérapies tissulaires et les substituts cutanés, sont au stade de développement et d’évaluation ou encore de recherche. Ces techniques sont surtout l’apanage des services spécialisés.
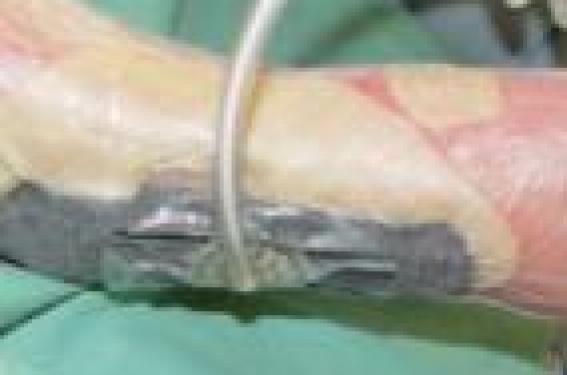
La thérapie par pression négative (TPN) La TPN est un concept introduit en 1986 par L.C. Argenta et M.J. Morykwas(1) aux États-Unis. La TPN consiste à délivrer sur une plaie une pression négative (sous-atmosphérique) au travers d’une structure spongieuse. Il s’agit plus précisément d’un bloc de mousse de polyuréthane ou de polyvinylalcool réticulé rendu étanche par un film adhésif transparent mis en place sur la plaie. Une force d’aspiration (pression négative) est alors appliquée à travers une tubulure placée sur la mousse grâce à une technologie contrôlée et sécurisée, appelée Vacuum assisted closure® (VAC®) et commercialisée par la société KCI. Le vide ainsi créé provoque des effets bénéfiques pour la plaie. La TPN favorise la cicatrisation, car elle permet d’éliminer les exsudats. Elle facilite la formation d’un tissu de granulation, rapproche les berges de la plaie, diminue la taille de celle-ci, améliore la perfusion dermique et favorise un environnement humide propice à la cicatrisation. Cette technique a fait l’objet de très nombreuses publications qui ont permis de vérifier ses effets bénéfiques dans de multiples situations cliniques comme les plaies traumatiques, les médiastinites, les plaies abdominales. Des résultats encourageants ont également été publiés dans le domaine des plaies chroniques (escarres, ulcères de jambe). Une étude multicentrique menée sous l’égide du ministère de la Santé est en train d’évaluer l’intérêt et le coût de cette technique par rapport aux procédés de cicatrisation plus classiques. • Conseils d’utilisation et contre-indications Les plaies infectées non détergées restent une contre-indication à cette technique, surtout s’il existe une arthrite ou ostéite sous-jacente non contrôlée. Il est donc recommandé, avant d’appliquer la TPN, de réaliser un bon débridement manuel afin d’éliminer les tissus nécrosés et/ou infectés, et de mettre en place une antibiothérapie générale adaptée en cas d’infection. Le pansement est renouvelé en général toutes les 48 heures. Un délai plus court de 24 h peut être adopté en cas de plaie très exsudative ou colonisée. Cette technique doit être mise en place par un personnel formé. Le choix des paramètres de réglage, la surveillance sont déterminants pour éviter tout accident. Figure 1. Traitement par pression négative : pansement d’ulcère de jambe mis en pression. Le PDGF-BB ou bécaplermine (Regranex®) Le PDGF est un facteur de croissance, puissant stimulant de la prolifération, du chémotactisme et de la synthèse des protéines des fibroblastes dermiques humains. C’est également un facteur chémotactique des neutrophiles, des monocytes et des cellules musculaires lisses migrant dans les plaies. Il est obtenu par recombinaison génétique. Il se présente sous forme d’un tube de 15 g renfermant 100 µg de PDGF-BB pour 1 g d’hydrogel. Le PDGF-BB (bécaplermine) a obtenu des résultats significatifs sur la cicatrisation d’ulcères du diabétique dans une étude randomisée portant sur 282 patients. Ceci lui a permis d’obtenir une AMM dans le traitement des ulcères diabétiques chroniques profonds d’origine neuropathique, non ischémiques, de surface 5 cm2, en association aux soins adaptés à la plaie. Il s’agit d’un médicament d’exception en raison de son coût élevé, remboursé à 65 % par la Sécurité sociale. • Précautions d’utilisation : produit à conserver impérativement entre + 2 et + 8 ° et utilisable 6 semaines après ouverture. Pansements à base de collagène Le Catrix® Il s’agit d’un mélange de 50 % de mucopolysaccharides et de 50 % de collagène de type II bovin, qui se présente sous la forme d’une poudre blanche. Approuvé par la Food and Drug Administration (FDA) pour le traitement des escarres, des ulcères de stases, des brûlures du 1er et 2e degrés, des ulcères du diabétique, des incisions postchirurgicales, des radiodermites et des plaies aiguës, il n’est pas disponible en officine en France, mais peut être commandé par les hôpitaux et cliniques. Il n’est donc pas remboursé, à ce jour, par la Sécurité sociale. Le Promogran® Le Promogran® (Johnson & Johnson) est la première matrice biorésorbable à effet régulateur sur les métalloprotéinases. Ce pansement est également protecteur des facteurs de croissance endogènes. Il est composé de cellulose oxydée, régénérée et de collagène. Il se transforme en gel lorsqu’il est en contact avec les exsudats de la plaie. Les métalloprotéinases sont des endopeptidases qui dégradent essentiellement la matrice extracellulaire et la membrane basale. Le Promogran® favorise la cicatrisation en inactivant l’excès de métalloprotéases. Il possède en plus des propriétés hémostatiques et antiradicalaires. Il est uniquement délivré à l’hôpital et se présente comme une matrice de 28 cm2 ou de 123 cm2. Non remboursé par la Sécurité sociale, il peut être utilisé dans les plaies détergées nécessitant une cicatrisation dirigée, exemptes de tissus nécrotiques : ulcères diabétiques, veineux ou mixtes, escarres, plaies traumatiques et postchirurgicales. Son coût est très élevé (environ 165 euros les 10 plaques de 28 cm2). De gauche à droite figures 2 à 4. Figure 2. Application par spray de gel plaquettaire sur un ulcère de jambe. Figure 3. Résultat du traitement par gel plaquettaire après 4 mois. Figure 4. Prélèvement d’un feuillet de kératinocytes autologues Epibase® sous-athmosphérique. Les voies de recherche Les facteurs de croissance Les facteurs de croissance (FC) sont des peptides synthétisés par les différents types cellulaires présents au cours de la réparation tissulaire. Ils servent à la communication ou à l’interaction des cellules entre elles ou avec la matrice extracellulaire. Ce sont des agents mitogènes, angiogénétiques, chémotactiques et/ou inducteurs de la synthèse protéique intervenant au cours des différentes phases de la cicatrisation cutanée sur les kératinocytes, les fibroblastes, les cellules endothéliales, les polynucléaires et les monocytes. Depuis les années 1990, de nombreux FC ont été fabriqués en quantité suffisante soit à partir d’un extrait animal, soit par génie génétique, soit à partir de produits autologues riches en FC. Dès lors, ils ont fait l’objet d’études cliniques évaluant leur efficacité dans des pathologies tels que les escarres, les ulcères de jambes et les maux perforants des diabétiques. Tous les facteurs de croissance suivants ont été étudiés de façon isolée : l’EGF, le GM-CSF, le TGFb2, le bFGF, le G-CSF, le KGF (répifermine), le PDGF-BB (Regranex®, cf. plus haut). Seuls ces deux derniers produits ont permis d’obtenir des résultats encourageants. Le KGF a montré, dans une étude randomisée portant sur 94 patients souffrant d’ulcères de jambe, une diminution significative de 75 % de la surface totale de la plaie. Les thérapies tissulaires l Les surnageants de plaquettes activées Ces surnageants sont préparés à partir du sang total du patient. Il s’agit dans la majorité des cas de produits autologues permettant, à l’aide de techniques plus ou moins complexes, d’obtenir des plaquettes activées in vitro par de la thrombine, elle aussi le plus souvent autologue. Les plaquettes, leucocytes et thrombocytes enfermés dans le réseau de fibrine, produisent et libèrent de nombreux facteurs de croissance : PDGF-BB, TGFb, bFGF, EGF intéressants dans la cicatrisation. Quelques études (présentées dans le tableau) ont soulevé notre intérêt. Dans notre service, nous avons également pu essayer deux de ces techniques avec des résultats parfois surprenants. Nous attendons bien entendu des essais de phase III pour étayer nos premières impressions. Un essai français est actuellement en cours sur l’intérêt des plaquettes autologues comme traitement adjuvant de la cicatrisation des ulcères veineux. l Les produits sanguins autologues Les produits sanguins autologues sont soit les surnageants plaquettaires que nous venons de citer, soit des cultures de cellules mononuclées autologues, replacées sur les plaies selon divers protocoles. Il est à notre avis beaucoup trop tôt pour pouvoir conclure sur ces thérapies, étant donné le faible nombre d’études cliniques disponibles et la divergence des résultats obtenus. l Les substituts cutanés Il existe trois grands types de substituts cutanés : – les cultures de kératinocytes ; – les matrices de collagène et protéoglycanes ; – les cultures de kératinocytes et/ou de fibroblastes humains allogéniques sur ou dans un biomatériel. • Les cultures de kératinocytes Elles sont utilisées dans les centres de grands brûlés et en chirurgie plastique. De nombreux modèles ont été développés. Celui de Green et Rheinwald, le plus ancien, puis celui de Barrandon, qui permet une meilleure manipulation du greffon cultivé en le plaçant sur un support de fibrine. Ces cultures d’épiderme sont également commercialisées. Citons, par exemple, Epibase® des Laboratoires Genévrier qui effectuent des essais de phase III dans des indications portant sur les plaies chroniques. Les cultures de kératinocytes nécessitent une technicité et une infrastructure importantes. Leur coût est élevé. Il faut attendre 3 semaines avant d’obtenir un nombre suffisant de greffons et la rétraction cutanée peut être relativement importante. • Le derme artificiel Un derme artificiel dépourvu d’élément cellulaire a été mis au point par Burke et Yannas. Il s’agit d’une matrice extracellulaire composée de collagène et de glycosaminoglycanes proches du derme normal. Cette matrice à l’avantage d’être stockable, donc rapidement disponible. Elle permet le recouvrement transitoire d’une zone excisée en attendant la culture de kératinocytes. Par exemple, une matrice est commercialisée sous le nom d’Intégra® (Integra lifesciences corporation). Elle se présente sous la forme d’une éponge de collagène acellulaire recouverte d’un film étanche de silicone qu’il conviendra de retirer juste avant de mettre l’autogreffe en place. La technique de pose doit être rigoureuse et laissée à des équipes entraînées. Le risque d’infection est non négligeable. La qualité secondaire de la peau s’en trouve nettement améliorée. • Culture de kératinocytes et/ou de fibroblastes Les substituts cutanés apportent une culture de kératinocytes et/ou de fibroblastes humains allogéniques sur ou dans un biomatériel. On distingue : – des substituts cutanés épidermiques comportant une culture de kératinocytes sur une matrice d’acide hyaluronique ; – des substituts cutanés dermiques contenant une culture de fibroblastes allogéniques dans une matrice de vicryl, résorbable en 2 à 4 semaines ; – des substituts cutanés « complets » contenant un compartiment épidermique (culture de kératinocytes allogéniques, issus de prépuce humain) sur un compartiment dermique formé de fibroblastes allogéniques, inclus dans une matrice de collagène bovin. Le débat entre l’origine des cellules allogéniques et/ou autologues est toujours au cœur de l’actualité. Notons que les cellules allogéniques sont immédiatement disponibles, alors qu’il existe un délai de 3 semaines environ entre la biopsie-source et l’obtention d’un premier greffon de kératinocytes autologues. Le clinicien pourrait être tenté de traiter une plaie chronique avec des cellules allogéniques jeunes ayant un pouvoir prolifératif et métabolique supérieur aux cellules de son malade souvent âgé et/ou débilité. Mais on sait actuellement que les kératinocytes, même s’ils ne synthétisent pas d’antigènes HLA-DR in vitro, sont progressivement rejetés pour être remplacés à long terme par ceux du receveur. Les substituts allogéniques ne peuvent donc plus être nommés « greffons », puisque leurs cellules n’ont pas la mission de s’incorporer au néo-tissu de manière définitive. Ces produits ont pour but de délivrer des molécules activant la cicatrisation et d’entrer par conséquent dans la classe des pansements biologiques actifs. C’est le cas d’Apligraf® commercialisé par Organogenis. Ce produit est constitué d’un composite de fibroblastes et de kératinocytes allogéniques, insérés dans une matrice de collagène bovin de type matrice en gel 3D. Il a obtenu l’AMM de la FDA : ulcères veineux et diabétiques. Dans une étude de Phillips(2), il existait une différence significative en termes de cicatrisation complète à la 24e semaine (57 % vs 40 %) et le produit avait disparu à 2 mois pour être remplacé par le propre tissu du receveur. Conclusion L’utilisation des feuillets de kératinocytes autologues pour le traitement des brûlures étendues récentes est actuellement la seule indication validée de la thérapie cellulaire. Les substituts cutanés font l’objet d’études cliniques, essentiellement sur des plaies chroniques et donnent des résultats encourageants. Dans l’avenir, il faudra privilégier les substituts cutanés autologues, aussi bien en raison de la sécurité sanitaire qu’en raison d’impératifs réglementaires ou économiques.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :