Publié le 19 déc 2010Lecture 13 min
Kératoses actiniques et champ de cancérisation
J. KANITAKIS, Clinique dermatologique, Groupement hospitalier Édouard Herriot, Lyon

Les kératoses actiniques sont des lésions cutanées fréquentes, correspondant à une étape précoce de la cancérogenèse cutanée, intermédiaire entre le champ de cancérisation, cliniquement invisible, et le carcinome spinocellulaire avéré. Leur traitement fait appel à des techniques destructrices classiques (notamment la cryothérapie), et de plus en plus à des techniques (photothérapie dynamique) ou à des médicaments (imiquimod, 5-fluoro-uracile), permettant ainsi de traiter simultanément le champ de cancérisation.
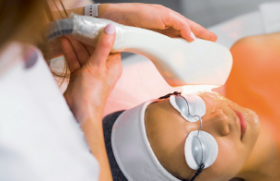
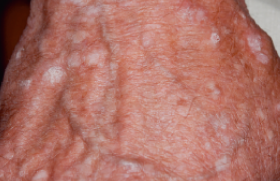
Aspects épidémiologiques Les kératoses actiniques (KA), également appelées kératoses séniles ou préépithéliomateuses ou précancéreuses, sont des lésions cutanées fréquentes, se présentant cliniquement comme des lésions érythémateuses brunâtres, plus ou moins kératosiques, parfois plus palpables que visibles, survenant sur des zones photoexposées (visage, cou, cuir chevelu de sujets chauves, dos des mains) de sujets adultes (en général de plus de 50 ans) à peau claire, souvent sur fond d’héliodermie. Ces lésions peuvent être uniques mais sont le plus souvent multiples et parfois confluentes. Elles semblent plus fréquentes chez les hommes, mais leur incidence précise est mal connue ; elle serait plus élevée dans les pays à fort ensoleillement, comme en Australie. Il semble que leur incidence globale soit en augmentation, en raison du vieillissement de la population, de l’augmentation de l’exposition solaire de celle-ci, liée à des activités de loisirs en plein air, et à l’augmentation de la population des personnes ayant une immunosuppression iatrogène (greffe d’organes, maladies auto-immunes) ; la diminution de l’épaisseur de la couche d’ozone pourrait également jouer un rôle dans le même sens. Les facteurs favorisant l’apparition des KA sont : l’exposition cumulée aux rayons solaires (essentiellement UVB), le phototype clair, l’immunosuppression, ainsi que certaines génodermatoses associées à une diminution de la protection intrinsèque de la peau aux effets mutagènes des rayons UV (Xeroderma pigmentosum, albinisme). Histologie Les KA sont caractérisées par une dysplasie de l’épiderme qui débute dans ses assises les plus profondes, s’étendant progressivement vers la surface, en épargnant (initialement) la partie intraépidermique des annexes (acrotrichiums et acrosyringiums). Dans les couches lésées, les kératinocytes ont des noyaux volumineux, hyperchromatiques, parfois polymorphes, atypiques ou quelquefois mitotiques ; ils tendent à perdre leur polarité, et forment au niveau de la couche basale des bourgeons qui envahissent progressivement le derme superficiel (figure 1). Figure 1. Aspect histologique d’une kératose actinique. Noter l’hyperkératose parakératosique, l’aspect dysplasique de l’épiderme interannexiel et le respect de la partie intraépidermique des annexes cutanées (acrosyringium, acrotrichium). Celui-ci présente une élastose plus ou moins marquée, reflétant les dégâts actiniques solaires. Des altérarions supplémentaires peuvent être observées, comme par exemple : – une acantholyse/dyskératose suprabasale, aboutissant à des fentes acantholytiques (KA acantholytique) ; – un infiltrat lichénoïde dermique (KA lichénoïde) ; – une poïkilocaryose comme la maladie de Bowen (KA bowénoïde) ; – une hyperkératose très marquée (KA hypertrophique, réalisant à l’extrême l’aspect d’une corne) ; – une hyperpigmentation mélanique (KA pigmentée) ; – une atrophie épidermique. Ces formes histologiques n’ont pour la plupart pas de traduction clinique particulière. À l’instar des lésions dysplasiques de la vulve (VIN : Vulvar Intraepithelial Neoplasia) et du pénis (PIN : Penile Intraepithelial Neoplasia), le terme de KIN (Keratinocytic Intraepidermal Neoplasia) a été proposé comme synonyme (histologique) de la KA, en distinguant les KIN en trois grades en fonction de l’épaisseur de l’épiderme affecté par les modifications dysplasiques (grade I : 1/3 inférieur de l’épiderme, grade II : 2/3 de l’épiderme, grade III : tout l’épiderme). Cette classification n’a cependant pas été unanimement adoptée. Kératose actinique : état précancéreux ou carcinome in situ ? La place nosologique des KA, notamment leur rapport avec les carcinomes spinocellulaires (CSC), est encore l’objet de nombreux débats. Selon le concept classique, les KA peuvent être la première étape d’un carcinome cutané, et à ce titre elles sont considérées comme des précurseurs de cancers, d’où les termes de « précancérose », de kératose « précancéreuse » ou « préépithéliomateuse ». Pour plusieurs auteurs, les KA peuvent longtemps rester stables, voire régresser spontanément. Certaines études ont évalué le taux de « progression » annuelle des KA en CSC, et ont rapporté des pourcentages faibles (< 10 %). Cependant, de plus en plus d’auteurs tendent à assimiler les KA à d’authentiques CSC in situ. En effet, il est très difficile, voire impossible, de tracer une limite nette (que ce soit sur le plan clinique, histologique ou moléculaire) entre KA et CSC. De plus en plus d’auteurs tendent à assimiler les kératoses actiniques à d’authentiques CSC in situ. Sur le plan clinique, certains signes ont été proposés comme des signaux d’alarme faisant suspecter une « transformation » d’une KA en CSC : induration ou infiltration, diamètre supérieur à 1 cm, augmentation rapide de taille, saignement, érythème, ulcération ; dans ces cas, une biopsie s’impose pour éliminer la possibilité d’un CSC déjà (micro-)invasif. En réalité, il est très difficile, voire impossible de distinguer cliniquement avec certitude une KA d’un CSC (débutant). Les facteurs prédisposants à ces deux entités sont les mêmes (exposition solaire cumulative, phototype clair, immunosuppression), qui partagent comme site de prédilection les zones photoexposées, plusieurs patients étant porteurs à la fois de KA et de CSC sur les mêmes zones. La limite histologique entre les deux entités peut également être difficile à définir. Par convention, on parle de KA lorsque la lésion est strictement intraépidermique, mais la présence de massifs tumoraux (micro-)invasifs peut être focale et échapper à l’examen histologique. Lorsqu’on examine de près les massifs tumoraux des CSC (invasifs), on constate que leurs cellules sont morphologiquement très proches, sinon identiques à ceux des KA avérées ; sur le plan architectural, les carcinomes micro-invasifs font le lien entre KA intraépidermique et CSC franchement invasif. La recherche de mutations de certains gènes intervenant dans la cancérisation cutanée (comme le gène p53, « gardien du génome » ou le gène CDKN2A) montre des différences quantitatives (mais pas qualitatives) entre KA et CSC. Il semble donc exister un continuum clinicohistologique et moléculaire entre la KA et les CSC. Toutes ces raisons font penser plusieurs auteurs que, plutôt qu’un état « précancéreux », les KA représentent d’authentiques carcinomes in situ, au même titre que la maladie de Bowen (avec laquelle elles partagent un aspect histologique souvent très proche). Certains gènes, comme le p53 ou le CDKN2A, interviennent dans la cancérisation cutanée. Faut-il traiter les kératoses actiniques ? Des controverses existent également quant à savoir si l’on doit traiter systématiquement toutes les KA. Les auteurs qui n’admettent pas l’assimilation des KA aux CSC in situ vont jusqu’à nier la nécessité de traiter systématiquement toutes les KA. Si l’on considère les KA comme des cancers in situ, l’intérêt de traiter ces lésions paraît évident. Cependant, même dans le cas opposé, il semble logique de traiter systématiquement les KA pour les raisons suivantes : – même en admettant que le risque annuel de « transformation » d’une KA individuelle en CSC soit faible, la multiplicité habituelle des KA chez un patient donné augmente considérablement le risque pour celui-ci de développer un CSC à court ou moyen terme ; – il n’est pas possible de prévoir quelle KA va évoluer vers un CSC (invasif), en dehors du fait qu’il est difficile ou impossible de différencier cliniquement avec certitude une KA d’un CSC ; – enfin, les KA sont affichantes et donc jugées inesthétiques par la plupart des patients, qui sont demandeurs de traitement. Récemment, le groupe de travail des Recommandations de pratique clinique sur le carcinome épidermoïde (spinocellulaire) a estimé qu’un traitement doit être proposé à tout patient présentant une KA en l’informant des modalités thérapeutiques disponibles. Il est aujourd’hui recommandé qu’un traitement doit être proposé à tout patient présentant une KA. Traitement Le traitement des KA fait appel à des méthodes classiques destructrices, visant à éliminer les KA déjà constituées et visibles cliniquement, et des traitements médicamenteux, introduits plus récemment, visant à éliminer les KA développées et à traiter le « champ de cancérisation » (voir plus bas). Les méthodes classiques comprennent : • La cryothérapie, technique très souvent utilisée car rapide, peu coûteuse, généralement bien tolérée. Elle a une bonne efficacité qui est cependant opérateurdépendante, mais ne prévient pas l’apparition de nouvelles lésions ; elle peut laisser des séquelles pigmentaires (hypopigmentation le plus souvent). • L’exérèse chirurgicale est possible mais au prix d’une cicatrice ; elle permet l’analyse histologique de la pièce d’exérèse, mais est peu pratique pour le traitement de KA multiples ; • Le curetage avec électrocoagulation, assez peu pratiqué en France ; • Le laser (à CO2 ou Erbium- YAG), coûteux, qui nécessite une anesthésie locale. Les traitements médicamenteux permettent de traiter non seulement des KA visibles, mais aussi des lésions infracliniques adjacentes du « champ de cancérisation ». La plupart d’entre elles sont relativement récentes : • Le 5-fluoro-uracile (5-FU) est un produit assez ancien montrant une bonne efficacité sur les KA, au prix cependant d’une irritation allant jusqu’à des érosions/ ulcérations plus ou moins douloureuses ; il présente un très bon rapport coût/efficacité/tolérance. • L’imiquimod (imidazoquinoline amine) est un agoniste du récepteur 7 « Toll-like » ; il agit en induisant la production de cytokines pro-inflammatoires par les cellules immunocompétentes cutanées. Il induit une inflammation importante, avec souvent révélation des lésions infracliniques en début de traitement. Cependant, les résultats à moyen et long terme sont très satisfaisants, même si l’efficacité du produit est patient-dépendante. L’imiquimod doit être utilisé prudemment chez les patients greffés en raison du risque (théorique) de réaction de rejet, bien que certaines études portant sur un nombre limité de patients greffés n’aient pas révélé de telles réactions, alors que le produit s’est avéré efficace. L’imiquimod a récemment obtenu l’AMM en France pour le traitement des KA (en plus des carcinomes basocellulaires superficiels). • La photothérapie dynamique (PTD) associe une application de produits photosensibilisants (méthylester de l’acide aminolévulinique [Metvixia®]) préalablement à l’irradiation du champ de cancérisation par une lumière visible. Il s’agit d’une technique coûteuse, non remboursable, encore assez peu accessible (en dehors de quelques services hospitaliers spécialisés). Elle peut être douloureuse mais permet d’obtenir de bons résultats, avec en plus un effet bénéfique sur les lésions d’héliodermie du visage. • Le diclofénac (anti-inflammatoire non stéroïdien inhibant la cyclo-oxygénase 2 qui intervient dans la cancérogenèse cutanée) associé à l’acide hyaluronique sous la forme d’un gel (Solaraze® 3 % gel) est moins irritant (mais aussi un peu moins efficace) que l’imiquimod. La stratégie thérapeutique dépendra du nombre de KA, de leur localisation, de leur caractère unique ou multiple et des caractéristiques du patient. La cryothérapie est conseillée en première intention pour les KA isolées ou en petit nombre, sur certaines localisations (vertex, oreilles, nez, joues, front, périorbitaires), ainsi que chez des patients peu autonomes. Le 5-FU, l’imiquimod ou la PTD seront proposés préférentiellement en cas de lésions multiples et/ou confluentes. Le gel de diclofénac sera proposé pour des KA périorbitaires. En cas d’échec à un traitement bien conduit, une biopsie devra être réalisée pour éliminer l’existence d’un carcinome déjà invasif. Le 5-FU, l’imiquimod ou la PTD sont proposés préférentiellement en cas de lésions multiples et/ou confluentes. Le « champ de cancérisation » Le concept de « champ de cancérisation » (« Field Cancerisation ») est relativement ancien puisque proposé par D. Slaughter (1944, 1953) sur la base d’observations cliniques sur les cancers oraux. Il repose sur la constatation du développement de multiples tumeurs sur un organe ou sur un même site anatomique, de façon synchrone ou métachrone. En effet, il est actuellement admis que l’effet d’un agent carcinogène donné s’exerce sur un ensemble de cellules d’une zone tissulaire, plutôt que sur une cellule isolée ; les tumeurs cancéreuses ne se développent pas suite à un événement cellulaire isolé, mais suite à un état anaplasique qui atteint simultanément un groupe de cellules (champ) d’un organe. Les tissus épithéliaux se situent à l’interface entre le milieu intérieur et le milieu extérieur et protègent l’organisme d’agressions externes, ils sont donc exposés continuellement à l’action de différents agents carcinogènes chimiques, viraux ou physiques (le rayonnement solaire, et plus particulièrement les UV en ce qui concerne la peau). Le concept de champ de cancérisation concerne les cancers de la peau, l’extrémité céphalique, la cavité orale, l’oesophage, l’estomac, le col utérin, le poumon, la vulve, la vessie, le côlon, le sein, les ovaires, le pancréas, et probablement aussi le cerveau et certaines hémopathies. Le champ de cancérisation de la peau correspond à la zone cutanée péritumorale (entourant des KA et CSC) comportant des anomalies infracliniques multifocales, pouvant être le lit de récidives ou de nouvelles lésions néoplasiques. La mise en évidence du champ de cancérisation n’est pas possible cliniquement, puisque les lésions sont par définition infracliniques. Figure 2. Plaques p53+ dans un champ de cancérisation : étape précoce du développement de kératoses actiniques/carcinomes spinocellulaires. La technique ULEV (Ultraviolet Light-Enhanced Visualisation, visualisation par amplification UV) permet de mettre en évidence des anomalies de la couche cornée et de la mélanisation épidermique, témoignant souvent de l’existence d’un état dysplasique. Sur le plan microscopique, le champ de cancérisation se caractérise par la présence d’atypies kératinocytaires plus ou moins discrètes, et la présence de groupes de kératinocytes exprimant le gène suppresseur de tumeurs p53 (« plaques » p53+) (figure 2). Deux étapes de la cascade de la cancérogenèse cutanée Sur le plan de la biologie moléculaire, les kératinocytes comportent des mutations de certains oncogènes (notamment CDKN2A/p16). La « cascade de cancérisation cutanée », correspondant à l’ensemble des modifications biologiques conduisant au développement d’une tumeur cutanée à partir d’une cellule normale, comprend les étapes successives de champ de cancérisation, les KA puis les CSC invasifs. Une conséquence clinique importante du champ de cancérisation est le fait que des récidives tumorales locales fréquentes sont observées après destruction d’une tumeur apparaissant sur un tel champ. Elles peuvent se produire sur le site même de la tumeur traitée, auquel cas la tumeur récidivante est génétiquement identique à la tumeur traitée, ou à quelque distance de la lésion primitive, auquel cas la tumeur est en règle génétiquement différente de la tumeur traitée. Ces faits peuvent inciter à traiter « préventivement » toute la surface d’une zone atteinte plutôt qu’à traiter individuellement chaque lésion. Conclusion Les kératoses actiniques représentent une étape précoce d’un carcinome spinocellulaire survenant sur terrain de cellules génétiquement modifiées, prédisposées à se transformer. Ce « champ de cancérisation », dû à l’action des rayons ultraviolets, est l’étape la plus précoce de la cascade de cancérisation cutanée, dont la prévention passe par des mesures de photoprotection. Si les traitements destructeurs des lésions individuelles (cryothérapie, notamment) sont encore largement utilisés, les nouveaux traitements permettent de traiter non seulement les lésions constituées mais aussi celles (infracliniques) du champ de cancérisation.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :