Publié le 27 fév 2019Lecture 6 min
Dermatite atopique de l’adulte - Une évolution thérapeutique ?
Michèle DEKER, Paris
Congrès JDP
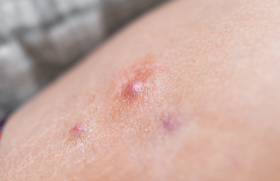
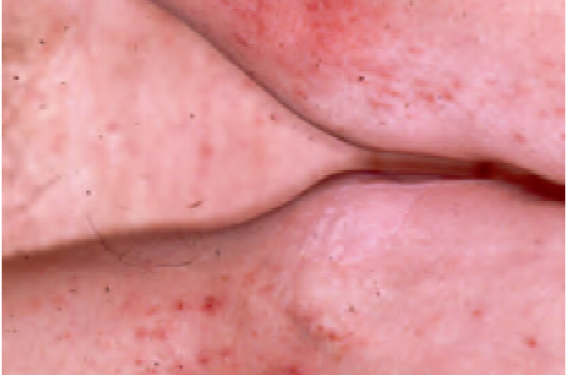
La dermatite atopique (DA) est une maladie fréquente et hétérogène, qui comporte néanmoins toujours des points communs. Elle est caractérisée par des altérations de la barrière épidermique et une inflammation de type 2 ; les kératinocytes sont la source et la cible de l’inflammation cutanée ; l’inflammation de type 2 implique l’immunité adaptative (LTh2) et innée (ILC2, éosinophiles, mastocytes, basophiles) ; l’IL4 et l’IL13, deux cytokines de type 2, induisent la réponse inflammatoire et les dysfonctions épidermiques de la DA.
Mise à jour de la physiopathologie dans la DA
L’altération de la barrière épidermique, d’origine génétique ou environnementale, favorise la pénétration d’allergènes, de bactéries, de polluants, etc. Ce phénomène entraîne l’activation des kératinocytes qui vont sécréter des substances inflammatoires, les alarmines (TSLP, IL25 et IL33). À leur tour, les alarmines activent les lymphocytes résidents (ILC2). Dans le même temps, des cellules de Langerhans sont activées et migrent dans les ganglions drainants où elles présentent les antigènes captés dans l’épiderme aux lymphocytes T. Sous l’effet des alarmines, ces lymphocytes vont se différencier en Th2, capables de sécréter de l’IL4, IL5, IL13 et IL31 (inflammation de type 2). Ce climat inflammatoire entraîne la suppression de la différenciation des kératinocytes, d’où une aggravation de l’altération de la barrière épidermique.
L’inflammation de type 2 est aujourd’hui définie comme une immunité de type 2, impliquant différents facteurs : facteurs d’agression ou insult (allergènes, bactéries, produits chimiques) ; facteurs déclenchants ou triggers (alarmines) ; cellules de type 2 (lymphocytes Th2 et lymphocytes innés (ILC2, innate lymphoid cells) ; cytokines de type 2 (IL4, IL5 et IL13) produites par les LTh2, ILC2, éosinophiles, mastocytes, basophiles et macrophages.
Il existe donc deux sous-populations de lymphocytes : Th2 issus de l’immunité adaptative, qui expriment des récepteurs spécifiques d’allergènes, et doués de mémoire ; des lymphocytes innés ILC2. L’activation des Th2 avec la sécrétion de cytokines IL4 et IL13 permet la différenciation des éosinophiles, leur recrutement au niveau des tissus cibles. Les ILC forment une famille très hétérogène, dérivée d’un progéniteur lymphoïde commun, qui se caractérise par l’absence de spécificité antigénique et sa sensibilité aux signaux de danger. Elles sont présentes en grande quantité dans la peau chez les patients ayant une DA, agissent en amont des Th2 et suffisent à produire une DA, même en l’absence de Th2, en cas d’altération de la barrière cutanée. Le taux de cytokines dans la peau et dans le sang est directement corrélé à la sévérité des altérations cutanées dans la dermatite atopique.
Des études transcriptomiques permettant d’identifier les signatures moléculaires dans la peau ont montré, chez les patients avec une DA traités par dupilumab, une normalisation des signaux inflammatoires. On peut donc considérer le dupilumab comme un immunocorrecteur.
Stratégie thérapeutique de la DA
Les émollients
Ils visent à réparer la barrière épidermique, en diminuant la xérose, les pertes insensibles en eau, et à améliorer le prurit et l’inconfort cutané. Ils traitent aussi la dysbiose. Il convient de les appliquer au moins une fois par jour, en bonne quantité, sur tout le corps et même en dehors des poussées. Les formules baume sont plus rémanentes. Il s’agit d’un traitement de 1re intention dans les DA légères et d’un traitement complémentaire indispensable dans les DA modérées et sévères.
Les traitements locaux de l’inflammation anti-Th2
Ils font appel aux dermocorticoïdes et aux inhibiteurs de calcineurine. Ils agissent en diminuant la présentation antigénique et le relargage des cytokines pro-inflammatoires. Ils doivent être appliqués lors des poussées et en traitement proactif. Il est important de dépister la corticophobie de la part des patients et des soignants. Le questionnaire TOPICOP, élaboré par l’équipe de Nantes, permet d’approcher ce problème. Le tacrolimus topique est souvent réservé aux zones « sensibles » (organes génitaux, visage) et pour une épargne cortisonique. En traitement proactif, on peut utiliser les dermocorticoïdes comme le tacrolimus topique (2 applications par semaine sur les zones de récurrence fréquente). Il convient de prévenir le patient des effets secondaires locaux (flush, brûlures avec le tacrolimus) et de le rassurer sur les risques (pas de risque accru de lymphome, de carcinome cutané ou autres tumeurs). Avant de déclarer l’échec du traitement local, il faut optimiser les mesures associées : éducation thérapeutique, arrêt des irritants locaux et des substances sensibilisantes, diagnostiquer un eczéma de contact allergique surajouté.
Quand le patient devient-il éligible à un traitement systémique ?
La question n’est pas complètement tranchée car la définition de l’échec n’est pas consensuelle. Les scores peuvent aider : SCORAD (sur 103), EASI (sur 72), DLQI (sur 30), score de prurit (1 à 10), IGA ou PGA (sur 4 ou 5) (tableau). Un algorithme a été proposé par les experts internationaux pour initier les traitements systémiques. En revanche, la définition de l’échec est variable selon les pays. Les Canadiens ont élaboré un consensus pour définir l’éligibilité au traitement systémique (encadré). Pour les Européens, la stratégie thérapeutique est fonction de la sévérité de la maladie évaluée par le SCORAD, sans prendre en compte la qualité de vie, le traitement systémique pouvant être décidé pour un score > 50.
En pratique, on pourrait définir l’échec des traitements locaux par la persistance de lésions/signes cliniques malgré un traitement bien conduit et l’éviction des facteurs aggravants, après réévaluation et éducation thérapeutique des patients si possible, et en cas de persistance d’un score d’activité de la maladie élevé et/ou d’une altération de la qualité de vie.
Les traitements systémiques conventionnels ayant l’AMM en France sont la photothérapie et la ciclosporine. Le méthotrexate, l’azathioprine et le mycophénolate n’ont pas l’AMM dans cette indication, mais ils sont utilisés. Ils ont toutefois fait l’objet d’études de taille restreinte, hormis la ciclosporine, comparativement au dupilumab, seul traitement ciblé disposant actuellement d’une AMM dans la DA. D’autres traitements ciblés sont en cours de développement (anti-Th2, antiprurit, petites molécules anti-inflammatoires antagonistes de JAK, etc.).
Résultats cliniques du dupilumab
Le dupilumab (Dupixent®), première biothérapie ciblée dans la DA, dispose d’une AMM depuis septembre 2017 dans le traitement de la DA modérée à sévère de l’adulte chez les patients éligibles à un traitement systémique, en cas d’échec ou d’intolérance ou de contre-indication à la ciclosporine. Le prix est attendu en vue de sa commercialisation.
Le dupilumab bloque une sousunité alpha du récepteur de l’IL4, commune au récepteur de l’IL13, deux cytokines majeures de type 2 responsables de la réponse inflammatoire. Le programme de développement a comporté deux études pivot de 16 semaines, SOLO 1 et SOLO 2, et SOLO CONTINUE, étude d’extension qui permettra de recueillir des résultats à long terme.
L’étude CHRONOS, multicentrique randomisée en double insu, a évalué pendant 52 semaines, chez des patients avec une DA en échec ou intolérants à la ciclosporine, l’efficacité et la tolérance du dupilumab versus placebo, associés aux dermocorticoïdes, à l’instar de la vie réelle. Le dupilumab a été administré, après une dose de charge de 600 mg, à la dose de 300 mg toutes les 2 semaines. À 16 semaines, plus d’un patient sur 3 sous dupilumab a été « blanchi » ou quasiment (IGA de 0 à 1), soit 39 % versus 12 %, et près de 2 patients sur 3 ont amélioré de 75 % leur score EASI, soit 69 % versus 23 %. À 52 semaines, une réduction significative de 90 % de l’intensité et de l’étendue des lésions (score EASI) est observée chez 51 % des patients traités par dupilumab, versus 16 %. Les scores de prurit et de qualité de vie sont également améliorés. Il n’a pas été observé de différence significative sur les effets indésirables comparativement au placebo. Les réactions au site d’injection sont mineures. Le traitement par dupilumab s’accompagne d’une réduction des infections cutanées (herpès, impétigination), comparativement au groupe placebo.
Dans l’étude CAFE, randomisée multicentrique, chez des patients soit naïfs, soit en échec de ciclosporine, et traités en association aux dermocorticoïdes, deux doses de dupilumab ont été évaluées. L’étude confirme l’amélioration des patients sous dupilumab : à la dose de 300 mg toutes les 2 semaines, près de 2 patients sur 3 ont amélioré significativement leur score EASI d’au moins 75 % à la 16e semaine et près d’1 patient sur 2 a présenté une diminution d’au moins 4 points du score de prurit.
En termes d’effets indésirables, il est observé un surcroît de conjonctivites ou de signes oculaires proches de la conjonctivite sous dupilumab, corrélé ou non à la préexistence de symptômes oculaires, dont le mécanisme à l’origine n’est pas élucidé. Les signes oculaires cèdent avec l’application de tacrolimus topique sur la paupière. Par ailleurs, le traitement par dupilumab peut s’accompagner d’une hyperéosinophilie (< 2 % des patients pour l’ensemble des essais cliniques), sans signe clinique d’infiltration des organes.
M. DEKER
D’après un symposium Sanofi Genzyme avec la participation de M. Bagot, D. Staumont-Salle, A. Nosbaum et A. Soria.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :