Maladie de système, Médecine interne
Publié le 05 sep 2011Lecture 14 min
La maladie de Lyme
Sur quels éléments cliniques et épidémiologiques fautil évoquer la borréliose de Lyme ? Quelle est la place des méthodes biologiques dans le diagnostic des manifestations de la borréliose de Lyme ? Quels traitements peuton recommander dans la borréliose de Lyme ? Quel est le suivi recommandé ? Quelles sont les mesures préventives à recommander ? Les réponses à ces questions s’appuieront principalement sur la 16e conférence de consensus en thérapeutique anti-infectieuse qui a traité de la borréliose de Lyme.
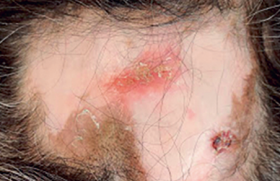
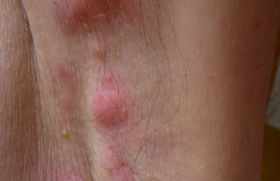
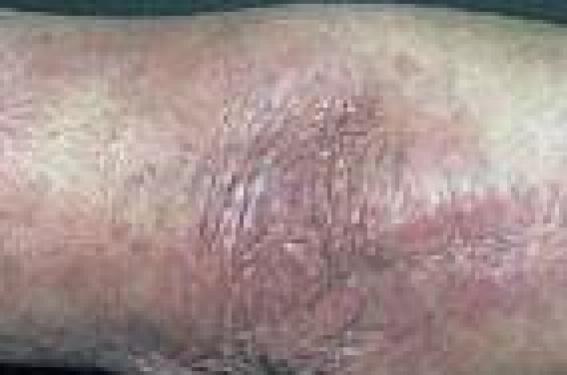
C. SORDET, Service de rhumatologie, CHU de Strasbourg Illustration/figure 1 : Érythème migrant : phase primaire de la maladie de Lyme. Épidémiologie La borréliose de Lyme est une zoonose transmise par morsure d’une tique du genre Ixodes due à une bactérie du genre Borrelia. Infection émergente en France, elle fait partie pour l’Institut national de veille sanitaire, des zoonoses non alimentaires prioritaires notamment du fait de sa fréquence (5 000 à 10 000 personnes infectées chaque année en France), de son risque potentiel de séquelles handicapantes et de l’existence d’un traitement précoce efficace permettant d’éviter la survenue de formes évoluées ou de complications ainsi que des possibilités de prévention. En Europe, où les études sont essentiellement séro-épidémiologiques, on note d’importantes variations géographiques avec globalement un gradient Est- Ouest. En France, l’incidence moyenne est estimée à 9,4 cas/ 100 000 habitants, avec des incidences plus élevées en Alsace et dans le Limousin. Une étude épidémiologique récente menée en Alsace confirme la forte incidence de la borréliose à 180 cas/ 100 000 habitants (1). L’agent pathogène, Borrelia burgdorferi sensu lato (Bb sl) appartient à l’ordre des spirochètes et au genre Borrelia. Le complexe Bb sensu lato comprend 12 espèces dont 6 sont considérées comme pathogènes pour l’homme : Bb sensu stricto, B garinii, B afzelii, B valaisiana, B lusitaniae, B spielmanii. Manifestations cliniques Phase primaire • L’érythème migrant (EM) (figure 1), qui est la manifestation la plus fréquente (40 à 77 %) et le plus évocatrice, apparaît en quelques jours à plusieurs semaines au site de la morsure de tique. Il existe de nombreuses variantes cliniques, mais classiquement il se présente sous la forme d’une plaque ovalaire de grande taille (> 5 cm) d’évolution centrifuge, le centre étant clair et les bords plus foncés ± infiltrés. Les formes multiples sont rares, elles traduisent une dissémination de l’infection(2). À ce stade, sont décrites des arthralgies dans 11 à 13 % des cas et des myalgies dans 9 à 12 %(3). La phase secondaire n’apparaît qu’en l’absence de traitement antibiotique de la phase primaire ou lorsque celle-ci est passée inaperçue. Ces signes apparaissent plusieurs semaines, voire plusieurs mois après le début de l’infection. Différentes manifestations cliniques sont alors possibles. Phase secondaire • Les neuroborrélioses précoces, dont 67 à 85 % sont des méningoradiculites(4) souvent de localisation crânienne, apparaissent 5 jours à 3 mois après la piqûre. Une réaction méningée est objectivée par la ponction lombaire, mais les manifestations cliniques sont rares. Les tableaux de myélite aiguë et d’encéphalite sont rares. • L’arthrite de Lyme est la forme majeure des manifestations articulaires de la borréliose de Lyme, elle est moins fréquente en Europe qu’aux États- Unis. Elle se caractérise par une monoarthrite ou une oligoarthrite d’apparition brusque touchant plutôt les grosses articulations, avec une atteinte prédominante pour le genou. • Le lymphocytome borrélien est rare (0,32 à 2,8 %) mais caractéristique. Il apparaît en moyenne 1 à 2 mois après piqûre de tique (de 2 jours à 6 mois). Il est plus fréquent chez l’enfant, et de localisation variée (scrotum, aréole mammaire, lobule de l’oreille, etc.). Il s’agit d’une plaque infiltrée ou d’un nodule indolore de 1 à 5 cm, de couleur variable allant du rose-rouge au brun-bleu. La confirmation histologique est nécessaire. L’examen histopathologique montre un nodule dermique constitué par un infiltrat lymphocytaire dense, souvent fait de follicules lymphocytaires bien délimités avec des centres germinatifs. L’immunomarquage est en faveur d’infiltrat lymphocytaire mixte à prédominance B, mais pouvant aussi contenir des macrophages, des plasmocytes et des éosinophiles. • Les manifestations cardiaques sont rares, elles apparaissent de 4 à 8 semaines après l’érythème migrant, se résument souvent à une myocardite a minima avec troubles de la conduction fluctuants et intermittents. Leur dépistage systématique n’est pas nécessaire. Figure 2. Acrodermatite atrophiante : phase tertiaire de la maladie de Lyme. • Les manifestations ophtalmologiques sont rapportées dans 1 % des cas. Les symptômes cliniques ne sont pas spécifiques, toutes les structures de l’oeil pouvant être touchées. L’arthrite de Lyme est moins fréquente en Europe qu’aux États-Unis. Phase tertiaire • Des manifestations neurologiques (< 10 % des neuroborrélioses) apparaissent dans un délai de plus de 6 mois après la piqûre. Elles sont de type encéphalomyélites chroniques (4 à 6 %)(5) ou encore polyneuropathies sensitives axonales. • L’acrodermatite chronique atrophiante (ACA) (figure 2) est observée chez l’adulte et en Europe. Elle peut débuter plusieurs mois, voire plusieurs années après la piqûre de tique. Elle évolue en 2 phases : inflammatoire (érythème bleu violacé plus ou moins infiltré et oedémateux, prédominant aux extrémités et en regard des articulations)( 6), puis une phase d’atrophie cutanée (peau fine et luisante en papier cigarette, laissant voir par transparence le réseau veineux). • Les arthrites chroniques sont rares et représentent moins de 10 % des formes articulaires aux États-Unis, leur incidence est inconnue en France et en Europe. Par ailleurs, de nombreux tableaux cliniques variés ont été décrits et associés à la borréliose de Lyme : polyneuropathies démyélinisantes, mononeuropathies multiples, syndromes extrapyramidaux, polyarthrites, enthésopathies axiales ou périphériques, morphée, lichens scléreux. Le caractère ponctuel de ces observations, avec seulement des données sérologiques pour soutenir le diagnostic, et l’amélioration uniquement partielle des symptômes sous antibiotiques ne permettent pas d’exclure une association fortuite. Diagnostic biologique de borréliose de Lyme Les différentes techniques du diagnostic de l’infection par Borrelia burgdorferi sont la recherche directe par la culture, la recherche génomique et la recherche indirecte par techniques immuno-enzymatiques de dépistage et d’immuno-empreinte. Les techniques directes • La culture d’un liquide biologique ou d’un prélèvement biopsique doit se faire dans des conditions strictes d’asepsie et sur un milieu de culture spécial appelé BSK (Barbour-Stoenner- Kelly). Le délai de positivité est long, le prélèvement doit être analysé jusqu’à 8 semaines avant de conclure à la négativité de la culture. Sa valeur prédictive est faible, mais sa sensibilité est estimée entre 50 à 80 % pour l’érythème migrant (EM), 60 % dans les acrodermatites chroniques atrophiantes (ACA). • L’amplification génique in vitro par PCR s’est fortement déve loppée depuis ces 10 dernières années, mais sa mise en oeuvre est délicate et reste l’affaire des laboratoires spécialisés. La sensibilité pour les biopsies cutanées d’EM est de 50 à 80 %(7) dans les ACA et d’environ 60 % pour l’arthrite de Lyme(8). Les techniques de PCR quantitative en temps réel sont de plus en plus utilisées, elles sont plus rapides que les techniques de PCR classique et permettent de déterminer l’espèce infectante. L’amplification génique in vitro par PCR s’est fortement développée depuis ces 10 dernières années, mais sa mise en oeuvre reste l’affaire des laboratoires spécialisés. Les techniques indirectes Elles permettent de révéler la présence d’anticorps dans le liquide biologique analysé. • Plusieurs générations de tests Elisa ont été commercialisées. Actuellement, le recours de tests utilisant des antigènes recombinants a pour but d’augmenter la sensibilité, en particulier dans les phases précoces de la maladie. La distinction entre les anticorps de type IgG et IgM permet une meilleure interprétation des résultats. Après le contage, on peut détecter des IgM après 4 à 6 semaines puis une séroconversion IgG 2 à 3 semaines plus tard. Il est important de savoir que la performance des tests est très variable(9), par exemple dans les neuroborrélioses, la sensibilité en IgG varie de 21 à 98 % et la spécificité varie de 69 à 99 % en IgG et de 70 à 100 % en IgM. • L’immuno-empreinte est utilisée pour confirmer une sérologie positive par la technique immuno-enzymatique. Son principe repose sur la séparation des antigènes de Borrelia sensu lato en fonction de leur poids moléculaire et permet donc d’objectiver la spécificité des anticorps. Mais il y a un manque de standardisation de ces tests, ce qui rend difficile la création de critères diagnostiques. Toute sérologie positive en technique immuno- enzymatique doit être confirmée par l’immuno-empreinte. Quelles méthodes de diagnostic biologique selon les différentes manifestations de la borréliose de Lyme ? Situations au cours desquelles la sérologie n’a pas d’indication : - les sujets asymptomatiques ou présentant des signes mineurs ; - le dépistage systématique des sujets exposés ; - une piqûre de tique sans manifestations cliniques ; - l’érythème migrant typique ; - le contrôle sérologique systématique des patients traités. En cas de suspicion de neuroborréliose, la sérologie est recommandée sur le sérum, mais il y a surtout une indication à rechercher des anticorps anti- Borrelia dans le LCR, qui permet de calculer l’index de synthèse intrathécale des IgG spécifiques. En cas d’index positif, la spécificité avoisine les 100 % (tableau 1). Dans les formes précoces, la sérologie peut être positive dans le LCR alors qu’elle est encore négative dans le sérum(10). Les techniques de recherche directe ne sont pas recommandées car elles ont peu d’intérêt. En cas de suspicion d’arthrite de Lyme, la sérologie dans le sérum est recommandée, mais n’a pas d’intérêt dans le liquide synovial. Sa sensibilité varie de 60 à 100 %. Un résultat négatif doit faire évoquer un autre diagnostic. En cas d’arthrite persistante ou récidivante après traitement antibiotique adéquate, la recherche directe par PCR et/ou culture peut-être utile(11). Traitements L’objectif du traitement antibiotique d’une borréliose de Lyme est l’éradication complète des Borrelia, quelle que soit leur localisation tissulaire. En pratique, l’objectif est donc la résolution complète des symptômes en relation avec l’infection. Ainsi, le suivi post-thérapeutique sera avant tout clinique et la négativation d’une sérologie borrélienne n’est pas l’objectif du traitement. Phase primaire Il est recommandé d’administrer le plus précocement possible dès la constatation des signes cliniques d’EM : – amoxicilline 1 g x 3 fois par jour ou doxycycline 100 mg x 2/j par voie orale et pendant 14 jours si EM est isolé ; – amoxicilline 1 g x 3 fois par jour ou doxycycline 100 mg x 2/j par voie orale et pendant 21 jours si EM est multiple ; – en cas d’allergie ou de contreindication aux β-lactamines et aux cyclines, l’azythomycine peut être proposée à la posologie de 500 mg/j en une prise orale pendant 10 jours. Administrés précocement, ils réduisent la durée de l’évolution de l’EM(12) et bloquent le développement de la réponse humorale. Moins de 10 % des cas d’EM traités évoluent vers une infection disséminée(13), dont le tableau semble de moindre sévérité que chez les sujets non traités lors de la phase d’infection précoce(12). La fréquence de la réaction de Jarish Herxheimer avec aggravation transitoire des symptômes peut être estimée à environ 15 % dans les études. C’est une réaction bénigne ne justifiant pas l’arrêt de l’antibiothérapie et dont le traitement est symptomatique. Le suivi post-traitement est uniquement clinique. Les signes cutanés peuvent mettre plusieurs semaines à disparaître après la fin du traitement sans que cela soit synonyme d’échec thérapeutique. Cela ne nécessite ni prolongation du traitement ni la prescription d’un nouvel antibiotique. Moins de 10 % des cas d’EM traités évoluent vers une infection disséminée, dont le tableau semble de moindre sévérité que chez les sujets non traités lors de la phase d’infection précoce. Phases secondaire et tertiaire (tableau 2) Dans les arthrites chroniques, l’utilisation de corticoïdes par voie intra-articulaire peut s’avérer utile après un traitement antibiotique bien conduit. Il n’y a pas d’essai thérapeutique randomisé portant spécifiquement sur les atteintes cardiaques, oculaires ou cutanées de la phase secondaire. Le traitement du lymphocytome borrélien est identique à celui de l’érythème migrant isolé avec une recommandation de traiter 21 jours. Pour le suivi, il consiste à surveiller l’efficacité des traitements sur les manifestations cliniques dont la résolution est d’autant plus lente et incomplète que le traitement a été mis en route tardivement. Il est donc pertinent de réévaluer la clinique au moins 2 mois après la fin de l’antibiothérapie. En cas de réponse partielle, il conviendra de discuter un traitement antibiotique complémentaire faisant appel à une autre famille antibiotique que celle du traitement initial. Le contrôle sérologique n’est pas recommandé. Mesures préventives • Les stratégies de prévention primaire en zone d’endémie ont pour but d’éviter le contact entre la tique et l’homme, et donc le risque de morsure. La plus simple à mettre en oeuvre est le port de vêtement long et de couleur claire permettant de mieux repérer les tiques encore non fixées sur la peau. L’inspection systématique de la peau et du cuir chevelu après exposition au risque de piqûre est primordiale. La piqûre de tique passe facilement inaperçue en raison de son caractère indolore dû au relargage de substances anesthésiantes et antiinflammatoires par les glandes salivaires de la tique. De plus, du fait de faible taille (1 à 3 mm), les nymphes qui sont la forme la plus fréquente à se fixer sur l’homme sont difficiles à repérer. L’utilisation de répulsifs naturels (citriodiol) ou de synthèse (DEET) peut être recommandée en zone d’endémie, en évitant le contact avec les yeux et les muqueuses sans dépasser plus de 3 applications/ jour. La vaccination était une stratégie de prévention utilisée aux États-Unis dans les années 1990 mais le vaccin Lymerix®, approuvé par la FDA en 1998, a été abandonné en 2002 en raison de son coût, de sa faible efficacité et de ses effets indésirables (arthrites)(14). D’autres projets de vaccins sont actuellement à l’étude. • Les mesures de prévention secondaire reposent essentiellement sur la recherche et le retrait de la tique dans les plus brefs délais. Il existe une relation entre la durée d’attachement et le risque de transmission de Borrelia par la tique. Globalement, le risque de transmission à l’homme en zone d’endémie est de 1 à 4 % et dépend du taux d’infestation des tiques par Borrelia. Le risque de transmission peut être de 12 à 32 % si le temps d’attachement de la tique est au moins de 72 h(15). Il est recommandé de retirer la tique mécaniquement avec une pincette ou mieux avec un outil appelé tiretique. Le retrait se faisant par traction perpendiculairement à la peau avec une rotation dans le sens anti-horaire en évitant d’arracher la tête de la tique. Il faut ensuite désinfecter la peau. Il est déconseillé d’utiliser une méthode de retrait « chimique » car ces produits sont susceptibles de provoquer une régurgitation et donc d’augmenter le risque de transmission. Il existe une relation entre la durée d’attachement et le risque de transmission de Borrelia par la tique. Une antibioprophylaxie peut éventuellement s’envisager chez les patients qui ont été piqués. Seulement 30 % des patients ayant une borréliose de Lyme se souviennent avoir été piqués. Deux stratégies ont été étudiées : antibioprophylaxie de type traitement curatif assez comparable au traitement curatif de l’érythème migrant ou antibioprophylaxie monodose par cycline. Dans la littérature, on ne trouve qu’une seule étude randomisée, contrôlée, en zone d’endémie comparant la doxycycline en dose unique (200 mg) à un placebo administré dans les 72 h qui ont suivi une piqûre par Ixodes scapularis aux États-Unis(16). Au total, 500 patients ont été suivis 6 semaines après une piqûre de tique, le taux d’infection a été de 0,4 % dans le groupe doxycycline versus 3,2 % dans le groupe placebo (p = 0,04). Ce suivi de courte durée n’a pas permis de savoir si cette prise en charge évitait les signes neuro logiques ou articulaires. L’analyse de la tolérance montre 30 % d’effets indésirables dans le groupe doxycycline et 11 % dans le groupe placebo. L’antibioprophylaxie ne doit pas être recommandée de façon systématique mais peut être discutée en zone d’endémie chez des sujets à risque élevé de contamination (multiples morsures, durée d’attachement supérieure à 48-72 h).
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :