Cas cliniques
Publié le 07 nov 2021Lecture 4 min
Formes inhabituelles de porphyrie érythropoïétique congénitale spontanément régressive : suivi de cas familiaux sur 28 ans
Omar BOUDGHENE STAMBOULI, CHU de Tlemcen (Algérie)*,**
Les porphyries héréditaires sont des maladies liées au déficit d’une des enzymes intervenant dans la voie métabolique de la biosynthèse de l’hème. la porphyrie érythropoïétique congénitale (PEC) ou maladie de Günther, la première connue des porphyries et parmi les plus rares, est secondaire à un déficit en uroporphyrinogène iii cosynthétase (uPG III cosynthétase). Ce déficit entraîne une accumulation de porphyrines isométriques de type I et de leurs précurseurs dans le sang, les urines et les selles, responsables de la symptomatologie, en particulier cutanée à type de photosensibilité.
De multiples mariages consanguins sur plusieurs générations dans une famille de la région de Tlemcen (Algérie) ont abouti à l’apparition de cette affection récessive chez 5 enfants dans 2 branches de la famille(1).
Observations
Nous présentons ici deux cas inhabituels de PEC familiale dont le diagnostic a été posé 28 ans auparavant(1). Les deux cas se caractérisent par une évolution spontanément régressive et, de surcroît, en l’absence de toute mesure de pho- toprotection dans un pays à fort ensoleillement comme l’Algérie. Amina et Abdelwahed (tableau 1), 12e et 13e enfants de parents consanguins originaires de Tlemcen, présentaient depuis la naissance des urines foncées, une photosensibilité modérée et une fragilité cutanée au moindre traumatisme.
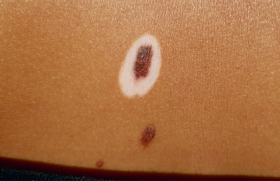
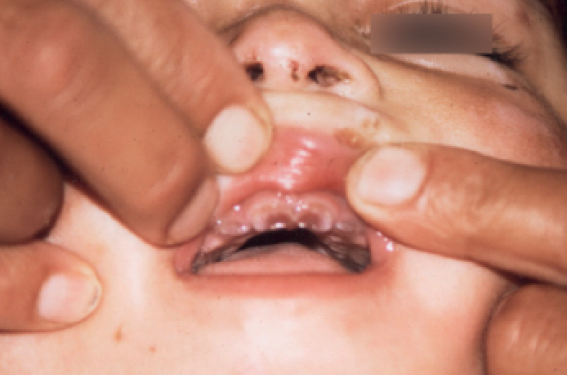
À l’âge de 18 mois, ils ont présenté des bulles sur les zones photo-exposées, des hyperpigmentations, une koïlonychie des ongles des orteils, une érythrodontie (figure 1) et une splénomégalie modérée.
Le diagnostic de porphyrie érythropoïétique congénitale était porté cliniquement, confirmé par les bilans biologiques (tableau2)(1).
L’uroporphyrinogène III synthétase (UROS III) était diminuée avec une augmentation de l’isomère I des uroporphyrines et des coproporphyrines dans les urines, les selles et les érythrocytes.
Nos deux malades avaient pour antécédent une sœur aînée, Fadela (figures 2 et 3), atteinte d’une forme plus sévère de PEC avec hypertrichose, érythrodontie, mutilation, atteinte osseuse des mains et splénomégalie. Fadela était décédée vers l’âge de 20 ans des suites d’une tuberculose pulmonaire.
Évolution
Après un suivi de 28 ans, les deux malades ne présentaient plus de lésions photosensibles : la recrudescence estivale de leur symptomatologie cutanée, nette au début, s’atténuait graduellement avec blanchiment complet après la puberté. L’examen clinique ne retrouvait qu’une hyperpigmentation des zones découvertes avec disparition de l’érythrodontie. Les urines étaient d’un aspect normal, non fluorescentes sous UV. L’imagerie ne retrouvait ni atteinte viscérale ni anomalie osseuse. Amina est actuellement étudiante en droit et Abdelwahed, menuisier. Ils mènent une vie tout à fait normale sans aucune précaution quant à l’exposition solaire.
Discussion
La PEC est une maladie génétique à transmission autosomique récessive, due à un déficit partiel ou subtotal en UROS III dont le gène se situe sur le chromosome 10q26(2). Le pronostic des formes sévères, avant l’avènement des premières greffes de moelle osseuse réussies, était redoutable.
Bien que le début de la pathologie soit précoce, ces deux malades présentent un phénotype clinique modérée semblable à celui observé dans les formes de PEC à révélation tardive. L’activité enzymatique résiduelle, mesurée à 18 mois, était d’environ 6 % alors qu’elle avoisinait 50 % chez les porteurs sains de la même famille, ce qui correspond aux données de la littérature.
La régression spontanée de la symptomatologie clinique chez ces deux malades, et paradoxalement après la puberté, période où les modifications hormonales entraînent une synthèse accrue de l’hème érythropoïétique et hépatique, laisse présumer de l’apparition d’un facteur protecteur contre l’élévation des porphyrines.
Dans une description récente d’une large famille de PEC, plusieurs enfants présentaient des signes cliniques sévères alors qu’un enfant, homozygote pour la mutation avec un déficit enzymatique profond, était apparemment sain. Cette observation se rapproche de la nôtre, mais elle en diffère par l’absence de signes cutanés depuis la naissance.
Conclusion
Notre observation est un autre exemple de l’hétérogénéité clinique interindividuelle de la PEC mais aussi de sa variabilité intra-individuelle chez les sujets atteints homozygotes. Une correction de la mutation de novo, avec restauration de l’activité enzymatique et correction des troubles métaboliques, ou l’influence d’un gène modificateur, qu’il soit dépendant ou distinct de la chaîne de biosynthèse de l’hème, protecteur de l’élévation des porphyrines, sont deux hypothèses attrayantes qui restent à élucider. Les porphyries sont des affections métaboliques qui ont beaucoup bénéficié des développements de la biochimie et de la biologie(3,4). Dans les pays du Maghreb, elles doivent être connues et répertoriées pour permettre notamment un conseil génétique.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :