Publié le 10 sep 2021Lecture 12 min
Le syndrome de Netherton : une génodermatose qu’il faut savoir évoquer
Nathalia BELLON, Paris
Le syndrome de Netherton est une maladie cutanée rare revêtant de multiples aspects pouvant associer une atteinte cutanée inflammatoire chronique évoluant par poussées, eczématiformes et/ou psoriasiformes, des anomalies pilaires, une prédisposition à l’atopie et notamment aux allergies alimentaires, un retard staturo-pondéral et de possibles complications systémiques. Les signes cutanés ou pilaires pathognomoniques doivent être connus de tout dermatologue.
Mécanismes cellulaires et moléculaires dans le SN.
D’après L. Furio et A. Hovnanian, Biol Chem 2014.
Le syndrome de Netherton (SN) est une maladie génétique rare dont l’incidence est d’environ 1/200 000 naissances. De transmission autosomique récessive, il est dû à des mutations dans le gène SPINK5 codant pour la protéine LEKTI (lympho-epithelial kazal type inhibitor), une anti-sérine protéase. Il est caractérisé par une atteinte cutanée inflammatoire variable : érythrodermie ichtyosiforme, ichtyose linéaire circonflexe, lésions érythématosquameuses, des anomalies pilaires de type trichorrexis invaginata et/ou alopécie partielle, et une prédisposition à l’atopie avec sensibilisations IgE et possibilité d’allergies alimenaires multiples(1).
PHYSIOPATHOLOGIE
La protéine LEKTI, d’expression ubiquitaire dans le corps humain, est principalement exprimée à l’état normal dans les épithéliums stratifiés, en particulier dans la couche granuleuse de l’épiderme. Elle inhibe l’activité de protéases telles que la trypsine, la plasmine, l’élastase ainsi que les peptidases associées aux kallicréines (KLKs). Dans le SN, les mutations de SPINK5 induisent une hyperactivité de ces protéases dans différents tissus, à l’origine de manifestations cliniques di- verses, dont les plus fréquentes sont les manifestations dermatologiques, atopiques et digestives. Ces manifestations sont dues à l’absence d’inhibition de la cascade protéolytique de KLK5, KLK7 et KLK14 en l’absence d’expression de LEKTI dans l’épiderme. Cette cascade conduit à la dégradation excessive des protéines composant les cornéodesmosomes (la desmogléine 1, la desmocolline 1 et la cornéodesmosine) et donc à une destruction accélérée de la couche cornée de la peau et à une altération des barrières épithéliales, dont la barrière cutanée. Ces perturbations et anomalies de barrières épithéliales (cutanée, digestive, nasale, buccale, génitale...) sont à l’origine de perturbations majeures du microbiote, notamment cutané, et jouent un rôle probablement majeur dans l’inflammation du SN. Il existe une grande variabilité phénotypique en partie liée à une corrélation génotype-phénotype. Les mutations c.153delT (p.gln52Lys fs* 6) concernant l’exon 3, fréquemment retrouvées en Turquie, sont à l’origine de formes plus sévères de SN et associées à un risque plus important de mortalité(1,2).
DIAGNOSTIC
Le diagnostic peut être fait dès la période néonatale, devant une atteinte cutanée évocatrice. Cependant, il n’est pas exceptionnel que le diagnostic soit évoqué plus tard dans l’enfance ou à l’âge adulte, après diagnostic de dermatite atopique ou de psoriasis, devant les similitudes de l’atteinte cutanée partagées entre l’une et l’autre de ces pathologies, et notamment dans les formes pauci-symptomatiques. Le diagnostic de syndrome de Netherton est confirmé par un tableau clinique évocateur associé à :
l’absence ou nette diminution d’expression de LEKTI en immunohistochimie sur une biopsie cutanée ;
et/ou la confirmation moléculaire (analyse génétique). La présence d’anomalies pilaires de type trichorrhexis invaginata (TI) en microscopie optique à lumière polarisée est également un argument diagnostique pathognomonique, qui peut permettre de surseoir à la biopsie cutanée. En revanche, l’absence de TI n’élimine en rien le diagnostic. Ces anomalies pilaires peuvent apparaître plus tardivement au cours de la vie(3).
MANIFESTATIONS CLINIQUES
La potentielle sévérité du SN, en particulier dans la première année de vie, peut mettre en jeu le pronostic vital. Il s’agit d’une véritable maladie systémique dont nous avons pu souligner la complexité à partir d’une série de 43 nourrissons suivis dans notre centre de référence MAGEC À Necker(4).
Dermatologiques
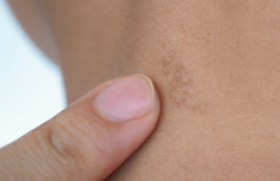
En période néonatale, l’atteinte est variable : lésions d’ichtyose linéaire circonflexe, décollements superficiels, inflammation cutanée non spécifique, desquamation fine, macération des plis jusqu’à l’érythrodermie. Il n’y a pas de membrane collodionnée à la naissance, donc l’aspect néonatal n’est pas celui d’un bébé collodion dans le SN. La précocité de l’atteinte cutanée, avec des lésions inflammatoires cutanées visibles dès les premiers jours de vie, permet d’évoquer ce diagnostic, par opposition notamment à la dermatite atopique (DA) qui survient généralement au-delà du premier mois de vie, même si les cas précoces dans un contexte d’allergie aux protéines de lait de vache sont possibles. Les lésions d’ichtyose linéaire circonflexe (figure 1), représentées par des lésions inflammatoires annulaires avec fine desquamation superficielle en double collerette en périphérie, sont quasiment pathognomoniques du SN, et doivent conduire à une biopsie cutanée pour marquage LEKTI en immunohistochimie.
Figure 1. Lésions d’ichtyose linéaire circonflexe
(service de dermatologie du Pr C Bodemer, CHU Necker-Enfants malades).
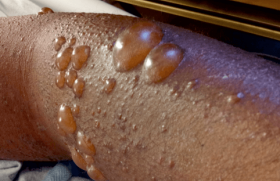
Les lésions inflammatoires, notamment en cas d’érythro-dermie (figure 2), peuvent être très érythémateuses, vernissées, avec possibilité de fissures cutanées. La xérose cutanée et la kératose pilaire sont fréquentes, d’intensité variable. L’aspect cutané est parfois brillant, œdématié, psoriasiforme, et parfois vésiculeux, eczématiforme.
Figure 2. Érythrodermie du SN et atteinte vésiculeuse et suintante du tronc
(service de dermatologie du Pr C. Bodemer, CHU Necker-Enfants malades).
L’atteinte péri-orificielle blépharite, atteinte péri-narinaire un peu lichénifiée, érythème et fissures péribuccales avec desquamation (« visage de clown ») – est fréquente (figure 3).
Figure 3. Atteinte du visage
(service de dermatologie du Pr C Bodemer, CHU Necker- Enfants malades).
Plus souvent retrouvée chez l’adolescent et l’adulte, mais parfois présente dès l’enfance, l’atteinte macérée des plis, et notamment du périnée, n’est pas rare, et certains patients développent une atteinte chronique érythémateuse et végétante, macérée, ou pseudo-cellulitique périnéale et axillaire (figure 4). Les anomalies pilaires, non systématiques, et d’intensité variable, sont caractérisées par des cheveux fins, courts, cassants, parfois brillants, accompagnés d’une alopécie diffuse de degré variable, et d’anomalies des poils dont sourcils et cils courts, peu fournis (figure 5).
Figure 4. Lésions axillaires érythémateuses lichénifiées,
macérées avec épaississement cutané marqué et fissures profondes
(service de dermatologie du Pr C. Bodemer, CHU Necker-Enfants malades).
Figure 5. Degrés variables de dysplasie pilaire et d’alopécie
(service de dermatologie, CHU Necker-Enfants malades).
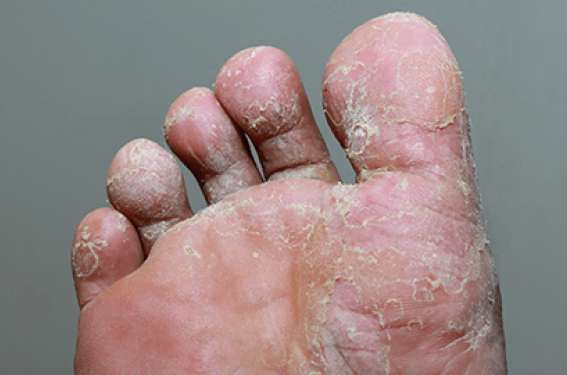
Des lésions desquamatives palmo-plantaires sont possibles, avec parfois un aspect très discret de kératodermie palmo-plantaire homogène, une lichénification des extrémités, un aspect de fine desquamation périphérique ou un aspect psoriasiforme (figure 6).
Figure 6. Desquamation des mains et lésions psoriasiformes des pieds
(service de dermatologie du Pr C. Bodemer, CHU Necker-Enfants malades).
Atopiques
Le SN constitue une prédisposition génétique aux manifestations atopiques. Les IgE totales peuvent être très nettement augmentées, avec une médiane allant de 84 kU/l [25-621] en période néonatale et augmentant au cours de la croissance jusqu’à 2 335,5 kU/l, [24.8- 35364] kU/L (données de cohorte du service de dermatologie de Necker). L’hyperéosinophilie, parfois majeure 3 (pouvant être > 8000/mm ), est fréquente. Ces sensibilisations IgE observées chez une majorité de patients ne sont pas toujours associées à des manifestations cliniques allergiques. Un certain nombre de patients développe des allergies alimentaires IgE médiées. Certains patients ont des allergies alimentaires retardées, à médiation cellulaire, avec des poussées inflammatoires cutanées ou des manifestations digestives induites par la consommation de certains aliments.
Il existe un surrisque d’asthme chez les patients SN par rapport à la population générale, qui ne semble pas être majeur par rapport au risque d’allergies alimentaires, se rapprochant du risque d’asthme chez un enfant atopique. La fréquence des rhinites allergiques chez les patients Netherton est difficile à évaluer du fait de l’absence d’expression de LEKTI dans la muqueuse nasale, à l’origine d’une rhinorrhée chronique fréquente. Les tests cutanés pour évaluation allergologique sont difficilement réalisables du fait de l’atteinte cutanée chronique et du risque de faux-positifs. La fréquence de sensibilisations de contact chez les patients avec SN n’a pas été évaluée, du fait notamment des difficultés de réalisation des tests épicutanés.
Digestives, ioniques et nutritionnelles
Une des complications classiques de la période néonatale dans les formes sévères est la déshydratation hypernatrémique. Celle-ci doit être recherchée régulièrement dans les premières semaines de vie, a fortiori en cas d’atteinte cutanée sévère, et doit être suspectée en cas de perte de poids. Sa survenue peut être tardive, parfois même au-delà de l’âge de un an, dans un contexte infectieux notamment. L’hypernatrémie sévère et prolongée est une cause de mortalité et de séquelles cognitives possibles. D’origine multifactorielle, le retard de croissance staturo-pondérale est fréquent. En période néonatale, des troubles de l’oralité, un inconfort cutané et digestif, des douleurs abdominales, des diarrhées profuses sont possibles, ce qui peut rendre nécessaire un support nutritionnel par sonde naso-gastrique, gastrostomie et/ou nutrition parentérale, pour une durée variable. Les déperditions hydriques, caloriques et protidiques peuvent être majeures, témoignant de la grande perméabilité des barrières épithéliales et de leur dysfonctionnement. Un reflux gastro-œsophagien sévère est possible. Des pathologies digestives à éosinophiles et un cas d’insuffisance pancréatique exocrine ont été décrits(5).
Infectieuses
Les complications infectieuses sont fréquentes. Les colonisations précoces pathogènes bactériennes et fongiques cutanées augmentent le risque d’infections cutanées, de macération, et surtout de septicémies à point de départ cutané chez les patients les plus fragiles. Les infections sur cathéter central, pour les patients concernés, sont fréquentes. D’autres complications infectieuses sévères (pneumonies, varicelle sévère, encéphalite à CMV...) ont été décrites, notamment en période néonatale, période de plus grande fragilité. L’expression de LEKTI à l’état normal dans le thymus, les déperditions protidiques et caloriques et les anomalies de barrières épithéliales expliquent en partie les anomalies immunologiques favorisant les infections chez certains patients avec SN sévère. Des hypogammaglobulinémies sont possibles.
Endocriniennes
Le retard statural est très fréquent, présent chez 58,3 % des patients à l’âge de un an et 48,6 % des patients au-delà dans notre cohorte (données en cours de publication). Plusieurs cas de déficit en hormone de croissance (GH) ont été rapportés. La mise en évidence de l’expression de LEKTI au sein de l’hypophyse à l’état normal laisse penser que le retard staturo-pondéral observé chez certains patients pourrait être directement lié à un dysfonctionnement de l’axe somatotrope. Une étude in vitro suggère que l’inactivation de LEKTI au sein du tissu hypophysaire pourrait entraîner un excès de destruction de la GH avant qu’elle n’atteigne la circulation générale(6).
Plusieurs cas de rachitisme (carentiels ou hyper-vitaminiques) ont également été rapportés. La protéine LEKTI est exprimée à l’état normal dans les parathyroïdes. Les patients peuvent également présenter une insuffisance corticotrope, qui peut en partie être reliée à la consommation de dermocorticoïdes.
Autres manifestations
Parmi les autres manifestations possibles, des hypertensions artérielles et des syndromes de détresse respiratoire aiguë en période néonatale ont été décrits(4).
PRINCIPALES COMPLICATIONS
Risque de déshydratation hypernatrémique en période néonatale.
Risque septique en période néonatale.
Allergies alimentaires fré- quentes, hyperIgE et hyper- éosinophilie.
Atteintes digestives, retard de croissance.
Atteintes endocriniennes : retard statural, déficit en GH ou résistance périphérique à la GH, rachitisme, insuffisance corticotrope.
Diagnostics différentiels
Parmi les diagnostics différentiels classiques, on peut citer la dermatite atopique, notamment en cas d’anomalies majeures des protéines de la barrière cutanée (dont anomalies de la filaggrine), le psoriasis, certaines ichtyoses congénitales impliquant d’autres protéines comme les protéines desmosomales (syndrome SAM : Severe skin dermatitis, multiple Allergies and Metabolic wasting lié à des mutations dans DSG1 ou de la desmoplakine(7)) ou d’autres formes d’érythrodermies ichtyosiformes (KRT10, ABCA12, etc.) ainsi que la dermite séborrhéique érythro-dermique de Leiner-Moussous. Une membrane collodionnée typique n’est jamais présente à la naissance dans un SN, contrairement à d’autres formes d’ichtyoses congénitales.
Des lésions de type ichtyose linéaire circonflexe sont possibles dans des pemphigus superficiels (anticorps anti-DSG1). Parmi les causes d’érythro-dermie néonatale, il faut bien sûr ne pas méconnaître un déficit immunitaire combiné sévère (SCID) : l’aspect histologique avec nécroses kératinocytaires et un phénotypage lymphocytaire permettent de confirmer ce diagnostic. La GVH materno-fœtale est également une cause rare d’érythrodermie néonatale. En période néonatale, les causes infectieuses d’érythrodermie doivent être évoquées : toxines staphylococciques, infection cutanée à Candida, notamment dans un contexte de déficit immunitaire. Des maladies métaboliques héréditaires (déficit multiple en carboxylases ou anomalies du cycle de l’urée) peuvent être révélées par un aspect érythémateux et des décollements cutanés(8).
PRISE EN CHARGE
La prise en charge est multi-disciplinaire et pour les formes sévères doit se faire en centre de référence. Les recommandations de prise en charge néonatale, parfois complexe, ont été publiées.
Dermatologique
Les émollients sont prescrits systématiquement afin de diminuer la xérose et d’améliorer le confort cutané. Le traitement des lésions inflammatoires cutanées, difficiles à traiter, repose sur l’usage de corticoïdes locaux, purs ou dilués dans une préparation émolliente, avec possibilité d’usage de tacrolimus topique. Les altérations de la barrière cutanée entraînant un risque important d’absorption percutanée des traitements, tout topique doit être prescrit et utilisé de façon mesurée, de préférence sur de courtes périodes, et quantifiée. Les antiprurigineux oraux peuvent être prescrits : les anti-histaminiques sont peu efficaces, mais l’hydroxyzine peut améliorer le sommeil en favorisant l’endormissement ; d’autres molécules comme la gabapentine ou la doxépine peuvent être essayées dans les cas d’un prurit sévère avec retentissement. Les antalgiques peuvent être utiles en période néonatale, mais sont rarement nécessaires au-delà. Les stratégies de décontamination microbienne et de désinfection cutanée sont utiles : antibiotiques locaux et/ou oraux adaptés à la flore cutanée et à l’antibiogramme, éventuellement par cures séquentielles, toilette antiseptique, antifongiques, etc.
Des traitements spécifiques ciblés sont à l’étude avec une efficacité variable, à mieux préciser : dupilumab (anti-IL4- IL13) chez l’adulte avec SN, ou biothérapies utilisées en traitement du psoriasis comme les anti-IL17 (secukinumab) ou anti- IL12-IL23 (ustekinumab). Les traitements anti-inflammatoires ou anti-prurigineux en cours de développement dans la dermatite atopique ou le psoriasis pourraient à l’avenir bénéficier aux patients avec SN.
Nutritionnelle, allergologique et gastro-entérologique
En période néonatale, les besoins hydriques, caloriques et protidiques peuvent être majeurs dans certains cas. Le recours à une nutrition entérale et/ou parentérale est parfois nécessaire. Les introductions alimentaires doivent être progressives, aliment par aliment, et au besoin guidées par les dosages d’IgE circulantes et tests cutanés si réalisables. Le régime alimentaire et les éventuelles évictions sont guidés par l’allergologue ou le dermato-allergologue. Une éviction précoce des protéines de lait de vache se discute au cas par cas. Non rares, les troubles de l’oralité (faible appétit, refus alimentaires multiples) doivent être dépistés précocement et pris en charge. Un reflux doit être suspecté en cas d’inconfort en période néonatale, en particulier en cas d’hospitalisation prolongée, et un traitement d’épreuve par IPP instauré. Un suivi régulier par un diététicien et un médecin nutritionniste sont également préconisés.
Endocrinienne
Un suivi régulier est préconisé, et systématique en cas de retard staturo-pondéral. En l’absence de rattrapage à l’âge de 5 ans il est justifié d’explorer l’axe somatotrope avec un dosage d’IGF1 et un test de stimulation de l’hormone de croissance. Un traitement par GH pourrait être discuté même en l’absence de déficit dans le cas d’un retard statural sévère, et a fortiori si le taux d’IGF1 est bas malgré un statut nutritionnel normal. Les insuffisances corticotropes ne sont pas rares et incitent à explorer de manière systématique les patients avec un dosage de cortisolémie à 8 heures et d’ACTH et, en cas de doute, un test au Synacthène. Une supplémentation systématique en vitamine D est nécessaire. Une surveillance régulière du bilan phosphocalcique dans les formes sévères, pour ne pas méconnaître un rachitisme non lié à une carence en vi- tamine D, mais secondaire à une carence en phosphore et calcium, s’impose.
Rééducatives
Chez l’enfant, dans les formes plus sévères, des évaluations régulières en kinésithérapie, ergothérapie, psychomotricité et/ou orthophonie permettent la mise en place de prises en charge adaptée aux séquelles, retards de développement ou troubles de l’oralité possibles.
EN PRATIQUE
Le syndrome de Netherton est une génodermatose rare, mais à connaître du fait de formes pauci-symptomatiques de diagnostic tardif, et du diagnostic rapide par immunomarquage cutané LEKTI ou examen des cheveux en lumière polarisée, en présence de signes spécifiques comme l’ichtyose linéaire circonflexe ou le trichorrhexis invaginata. Les possibles atteintes systémiques, notamment endocriniennes, sont à connaître. La période néonatale est une période de grande fragilité et de surrisque de mortalité. Le praticien doit garder en tête que la perméabilité cutanée majeure dans le SN favorise le passage systémique de tout topique appliqué.
NB : L’association Ichtyose France est une association impliquée pour le SN.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :