Cancérologie
Publié le 27 fév 2019Lecture 4 min
Prise en charge des mélanomes du stade précoce au stade métastatique
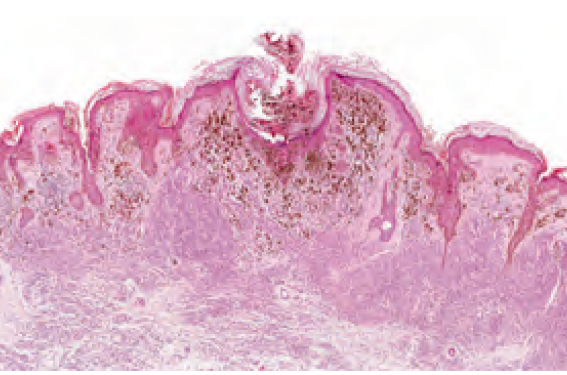
Congrès JDP
Nous sommes passés en moins de 10 ans d’une période où les possibilités thérapeutiques étaient restreintes dans le mélanome et le pronostic désespérant – avec une médiane de survie de 6 mois et une survie sans progression de moins de 2 mois – à l’émergence des thérapies ciblées et de l’immunothérapie qui révolutionnent le pronostic. Depuis 2011, 10 molécules ont été approuvées. Les résultats les plus spectaculaires sont obtenus par les thérapies ciblées, mais les immunothérapies prennent le pas sur la durée en permettant des survies prolongées. Aujourd’hui, ces mêmes traitements sont testés en situation adjuvante. Il reste néanmoins à trouver des biomarqueurs, à combattre les résistances, à s’intéresser aux patients porteurs de métastases cérébrales, entre autres.
Prise en charge en situation adjuvante
Les essais de traitement adjuvant, démarche thérapeutique validée pour la plupart des cancers, étaient peu convaincants dans le mélanome à l’ère de l’interféron – gain en survie sans récidive mais pas de gain en survie globale, et au prix d’effets secondaires. Les résultats spectaculaires observés avec les nouveaux traitements du mélanome au stade métastatique ont incité à les introduire plus précocement à un stade où la charge tumorale est plus faible, après traitement chirurgical. La plupart des molécules intéressantes au stade métastatique ont été évaluées en situation adjuvante.
L’ipilimumab (10 mg/kg), qui ne dispose pas de l’AMM en France dans cette indication, a toutefois été utilisé aux États-Unis. Il a été observé près de 29 % d’arrêts de traitement en raison de récidives (vs 60 % sous placebo) et 53 % d’arrêts à cause d’effets indésirables (vs 4,6 %).
L’étude du nivolumab, chez 906 patients en stades IIIB-IIIC et IV dont 41 % BRAF mutés, a bouleversé les concepts. Administré à la dose de 3 mg/kg tous les 15 j après résection chirurgicale, le nivolumab a permis une survie sans progression de 70,5 % à 12 mois versus 60,8 % chez les patients traités par ipilimumab, avec 3 fois moins d’effets secondaires de grade 3-4. Le pembrolizumab a montré des résultats similaires au nivolumab dans une étude versus placebo chez 1 019 patients en stade III. Les résultats de la deuxième partie de cette étude – cross over chez les patients en rechute – sont très attendus ; ils permettront de répondre à la question : vaut-il mieux traiter rapidement après la chirurgie ou attendre la rechute ?
Chez les patients mutés BRAF, il est possible de cibler l’oncogène muté (40 % des patients). Une étude comparant l’association dabrafénib (BRAF inhibiteur) et tramétinib (MEK inhibiteur) versus placebo chez 870 patients porteurs d’un mélanome stade III muté BRAF, a montré un gain en survie sans récidive à 3 ans (59 % vs 40 % ; le taux de guérison calculé serait de 54 % pour la thérapie ciblée vs 37 % pour le placebo à 4 ans. À noter cependant des effets secondaires de grade 3-4 dans 41 % des cas (vs 14 %) avec un arrêt pour toxicité dans un quart des cas.
Prise en charge au stade avancé
Dans les mélanomes mutés BRAF, les combinaisons anti-BRAF + anti-MEK donnent de meilleurs résultats que les anti-BRAF en monothérapie. Quel que soit le statut mutationnel BRAF, on peut traiter les patients par une immunothérapie ou un anti-PD1 en monothérapie ou associé à un anti-CTLA-4. En France, il n’est toutefois pas possible de prescrire l’ipilimumab qui n’est pas remboursé. La combinaison est nettement plus toxique (60 % de grades sévères vs 15 % avec la monothérapie anti-PD1).
L’évolution des traitements s’oriente dans plusieurs directions : au-delà du choix des molécules, vers une adaptation des doses, un mode d’administration différent, notamment en intratumoral, et le timing des traitements.
Concernant l’ipilimumab, grâce au suivi à long terme des essais, nous savons qu’il existe un effet-dose en termes d’efficacité (qui n’existe pas avec les anti-PD1), et de toxicité.
Un essai évaluant la combinaison ipilimumab + nivolumab a testé deux doses différentes d’ipilimumab (1 et 3 mg/kg) en double insu suivie d’une phase en ouvert à dose constante de nivolumab. Il n’y a pas de différence en survie sans progression et survie globale entre les deux bras, alors que l’incidence des effets secondaires est réduite dans le bras ipilimumab à faible dose.
D’autres combinaisons d’anti-PD1 avec des activateurs de l’immunité innée sont à l’essai, avec des résultats encourageants : des agonistes des Toll-like récepteurs (TLR-9), le virus oncolytique dérivé du virus herpès, TVEC, injecté dans les métastases, qui a la particularité de recruter des lymphocytes, et l’IL2 pégylée.
En termes de mode d’administration, l’immunothérapie intratumorale a récemment fait l’objet de recommandations d’experts (Marabelle A et al. Ann Oncol 2018 ; 29 : 2163-74).
Le timing est important quand on sait que les cancers se modifient, comme permettent de le déterminer des techniques ultra sophistiquées. Dans cette optique, une approche séquentielle du traitement est étudiée dans le cadre d’un essai européen (EORTC 1216) qui compare jusqu’à progression : une phase d’induction de 3 mois par encorafenib + binimetinib, suivie d’une combinaison nivolumab + ipilimumab, à la combinaison nivolumab + ipilimumab seule, chez des patients ayant un mélanome muté BRAF non résécable ou métastatique.
Au total
Nous disposons de deux types de traitement du mélanome métastatique : l’immunothérapie par anti-PD1 ou la combinaison ipilimumab + nivolumab ; le traitement combinant anti-BRAF + anti-MEK en cas de mélanome muté BRAF.
Les recherches s’orientent aujourd’hui vers une optimisation du rapport bénéfice/risque par l’adaptation des doses et des séquences de traitement, vers les combinaisons avec des activateurs de l’immunité innée et la recherche de biomarqueurs afin de mieux cibler les populations de patients.
D’après un symposium Bristol-Myers-Squibb avec la participation de V. Lebbé, D. Giacchero et C. Robert
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :