Dermatologie générale
Publié le 20 avr 2017Lecture 8 min
Conduite à tenir devant un condylome de l'adulte
Olivier AYNAUD, Hôpital Cochin, Paris
La condylomatose, décrite et prise en charge depuis l’Antiquité, est majoritairement associée à des papillomavirus humains (HPV) de génotypes faiblement oncogènes, HPV 6, 11, 42, etc., ceux-ci ayant un tropisme pour les kératinocytes de l’épithélium malpighien, donc sur toute la sphère ano-génitale, voire bucco-pharyngée.
Après le dépistage clinique de lésions sur l’ensemble de la sphère ano-génitale, l’approche thérapeutique doit être adaptée en fonction de leur localisation anatomique, de leurs aspects cliniques (lésions extensives, kératinisées, planes, etc.).
Cette conduite à tenir d’une condylomatose s’inscrit aussi dans le contexte clinique et/ou des pathologies associées du (de la) patient(e), c’est-à-dire patients(es) VIH, greffés(es), maladies auto-immunes qui peuvent développer des lésions ultifocales.
Un dépistage ano-génital complet
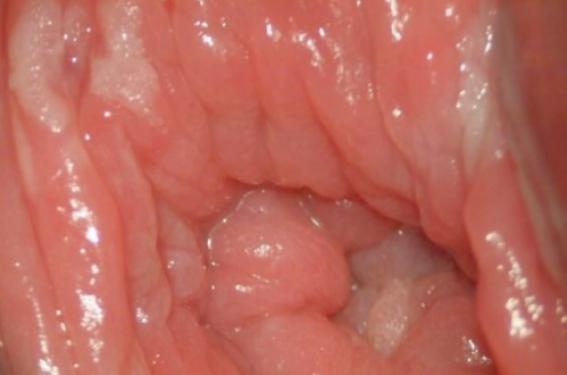
L’expression clinique d’une condylomatose est la présence de lésions exophytiques, forme la plus fréquente, mais aussi de lésions endophytiques, qui peuvent coexister et sont révélées par le test à l’acide acétique à 5 %. Dans le cadre de ce dépistage clinique, il est nécessaire de connaître les habitudes des comportements sexuels du (de la) patient(e) afin de repérer les zones anatomiques à risque de développement des condylomes. L’utilisation d’une loupe ou d’un colposcope permet le repérage des petites lésions condylomateuses des muqueuses (figure 1). Par ailleurs, comme la condylomatose ano-génitale est une infection sexuellement transmissible, il est nécessaire de demander un bilan des IST pour la personne infectée et son (sa) partenaire.
Figure 1. Condylomes vestibulo-vaginaux (vision colposcopique).
Chez l’homme, mais aussi chez la femme, la présence de lésions condylomateuses au niveau des muqueuses génitales externes amène le praticien à ne pas oublier d’examiner la sphère méato-urétrale masculine ou méatique chez la femme (figures 2 et 3). Cette localisation méato-urétrale des condylomes est plus fréquente chez l’homme, environ 8 à 12 % des hommes ayant une condylomatose génitale versus 2 à 4 % chez la femme. Par ailleurs, 40 % des hommes développent des lésions urétrales sans développer de lésions cliniques balano-préputiales. Pour dépister cette localisation lésionnelle, le praticien s’aide soit d’une pince longuette, soit d’un spéculum nasal de Hartmann, car 95 % des lésions HPV siègent dans la portion balanique de l’urètre soit au niveau de la fossette naviculaire, c’est-à-dire dans les 20 premiers millimètres, donc dépistable sous la vision colposcopique.
Figure 2. condylome de la fossette naviculaire urétrale.
Figure 3. Condylomes vestibulaire, méato-urétral accessibles par laser CO2.
Cette méthode de dépistage ne nécessite pas de faire une urétroscopie systématique lors de la présence de condylomes. L’urétroscopie doit être réservée aux patients présentant des récidives de lésions HPV urétrales après des traitements ou en présence de pathologies associées favorisant une immunodépression. La question du dépistage de lésions HPV urétrales par une cytobrosse urétrale pour génotypage HPV reste encore à évaluer.
La présence de condylomes de la marge anale doit faire rechercher des lésions HPV au niveau du canal anal, même si le(la) patient(e) n’a pas eu de relation sexuelle (figure 4).
Figure 4. Condylome du canal anal : traitement par cryothérapie,
électrocoagulation, laser CO2.
Ces lésions sont dépistées en pratiquant soit une anuscopie simple, soit, de préférence, par une anuscopie dite « de haute résolution (HR) ». Cette anuscopie HR se pratique sous vision colposcopique avec l’application d’acide acétique à 5 % et de lugol permettant de repérer des lésions condylomateuses planes. Dans notre série, 30 % des femmes ayant des condylomes ano-génitaux ont des lésions HPV du canal anal (figure 4). Cette anuscopie HR permet de pratiquer une biopsie, car l’aspect clinique exophytique d’une lésion intracanalaire n’est pas spécifique d’un condylome, d’autant plus si le(la) patient(e) est en immunodépression. Si les condylomes ano-génitaux sont à 90 % induits par les génotypes HPV 6 ou 11, des co-infections avec des génotypes HPV 16, 18, 31, 33 et 35 sont aussi retrouvées dans 31 % des condylomes ano-génitaux(1).
Par ailleurs, le frottis du canal anal peut être un outil de dépistage permettant de cibler les patients(es) pouvant bénéficier d’une anuscopie haute résolution.
Dans le contexte d’une condylomatose périnéo-vulvaire, un frottis cervical devra être pratiqué si celui-ci a plus d’un an mais après le traitement des condylomes, d’autant qu’une CIN peut être concomitante d’une condylomatose ano-génitale : 19 % des femmes avec une condylomatose périnéo-vulvaire ont un CIN de bas grade et 8,5 % un CIN de haut grade(2). Sinon, en présence de condylomes périnéo-vulvaires, un examen cervico-vaginal sous vision colposcopique avec l’application d’acide acétique et de lugol permet le dépistage de condylomes cervicaux et/ou vaginaux (figures 5 et 6).
Figure 5. Condylome du col utérin : traitement par cryothérapie,
électrocoagulation, laser CO2.
Figure 6. Condylomes vaginaux : traitement par laser CO2
de préférence sous colposcopie.
L’expression exubérante de la condylomatose de type Buschke-Lowenstein doit faire rechercher un facteur d’immunosuppression ou une pathologie concomitante en dehors d’un retard de consultation. Le praticien doit être particulièrement vigilant chez les patients(es) présentant une immunodépression virale, thérapeutique ou une pathologie auto-immune. Ces populations présentent un risque accru de développer une condylomatose multifocale et/ou des co-infections HPV, c’est-à-dire de présenter des condylomes associant une néoplasie intraépithéliale vulvaire, pénienne ou anale. D’où l’importance d’un examen ano-génital complet avec méatoscopie, anuscopie et colposcopie.
Approche thérapeutique
Les traitements d’une condylomatose ano-génitale dépendent de la localisation des lésions HPV, de leurs aspects cliniques, exophytiques ou endophytiques, et de leur diffusion, lésions extensives, multifocales. L’arsenal thérapeutique est soit chimique (acide trichloracétique, podophylline, 5-fluoro-uracile), soit immunologique (imiquimod), soit thermique (cryothérapie, électrocoagulation, laser CO2), voire chirurgical. Par ailleurs, il est important d’aborder ces traitements avec la notion de récidive et de récurrence(3). Si le condylome réapparaît sur un condylome traité préalablement, nous sommes dans le cadre d’une récidive et il est donc préférable de changer le type de traitement. En revanche, si un condylome réapparaît sur une autre zone que celle préalablement traitée, nous sommes dans le cadre d’une récurrence et donc le traitement initial a été efficace. Il est important de présenter aux patient(e)s cette notion de récidive/récurrence afin de les préparer au risque de traitements sur plusieurs mois. Nous proposons souvent un contrôle à 6 semaines puis 12 semaines.
Dans le cadre d’une condylomatose ano-génitale modérée, l’utilisation de l’imiquimod sur une période de 6 à 8 semaines donne des résultats satisfaisants dans 50 à 70 % des cas. Des réactions locales inflammatoires, y compris rougeurs, irritation, induration, ulcération/érosions et vésicules, peuvent se produire avec l’utilisation de l’imiquimod et l’hypopigmentation a également été décrite(4). La grossesse peut favoriser une condylomatose anogénitale qui est traitée référentiellement par des traitements thermiques, en particulier le laser CO2 entre la 28e et la 32e semaine d’aménorrhée, permettant une cicatrisation avant l’accouchement et de pratiquer une seconde séance si récidive.
La fréquence d’une papillomatose laryngée juvénile est faible, de l’ordre 1/1 500. Le traitement des condylomes ano-génitaux avec imiquimod pendant la grossesse semble être prometteur et ne pas compromettre une bonne issue de la grossesse, mais l'imiquimod n’a pas d’AMM dans cette indication.
Lorsque les lésions sont peu nombreuses et localisées au niveau de la muqueuse génitale, l’application d’acide trichloracétique à 70 % ou de la condyline (contre-indiqué lors d’une grossesse) sont aussi des traitements simples et satisfaisants dans 60 % des cas ; tout comme la cryothérapie, l’électrocoagulation ou le laser CO2 qui permet un traitement plus facile des condylomes de la sphère anale et des condylomes kératinisés, verruqueux.
Dans une condylomatose, diffuse, circonférentielle au niveau de la jonction cutanéomuqueuse du prépuce, nous proposons souvent en première intention la posthectomie, car l’application d’imiquimod ou la cryothérapie, l’électrocoagulation et le laser entraînent, dans la majorité des cas, un phimosis dont le traitement est l’exérèse du prépuce. Chez la femme, nous pouvons aussi être amenés à pratiquer une nymphectomie lorsque la condylomatose est diffuse au niveau des petites lèvres et imiquimod-résistante. En revanche, la chirurgie est proposée en première intention dans la condylomatose exubérante de type condylome géant et tumeur de Buschke-Lowenstein. Les condylomes urétraux sont traités, en fonction de leur localisation, par cryothérapie ou électrocoagulation pour des lésions méatiques en contrôlant l’absence de lésions plus en profondeur dans l’urètre. Pour les condylomes au niveau de la fossette naviculaire, l’utilisation du laser CO2 sous endoscopie est le traitement le mieux adapté. Certains auteurs ont traité des lésions HPV urétrales avec le 5-fluoro-uracile en crème avec quelques résultats satisfaisants.
Pour la condylomatose du canal anal, les traitements thermiques sous anuscopie haute résolution restent l’approche thérapeutique de choix, surtout par le laser CO2 permet tant de maîtriser la profondeur de l’évidemment, tout comme dans le cadre d’une condylomatose vulvaire avec une extension cervico-vaginale où les lésions sont traitées par laser CO2 sous vision colposcopique après avoir pratiqué une biopsie cervicale ou vaginale.
Le dernier champ dans une conduite à tenir devant une condylomatose ano-génitale est l’approche préventive pour le(la) partenaire. L’utilisation du préservatif garde une efficacité en présence de lésions cliniques HPV et pour les autres IST(5). Sinon la prévention primaire passe par la vaccination anti-HPV.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :