Maladie de système, Médecine interne
Publié le 31 oct 2022Lecture 4 min
Lupus érythémateux Un large éventail de médicaments candidats
Caroline GUIGNOT, Lille
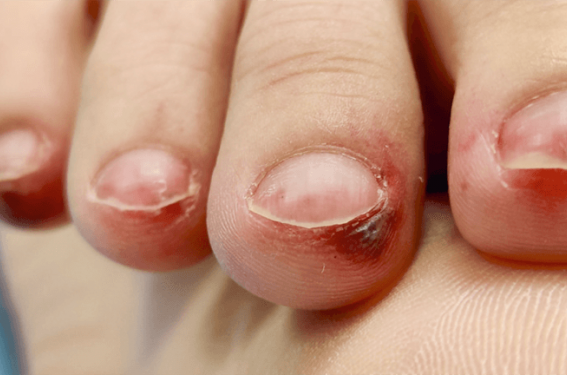
Depuis que les processus auto-immuns liés au lupus érythémateux systémique et cutané sont mieux compris, la recherche thérapeutique visant à développer d’autres options aux immunosuppresseurs s’accélère. Près d’une cinquantaine de solutions seraient aujourd’hui dans les tuyaux...
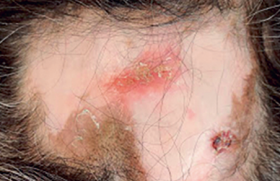
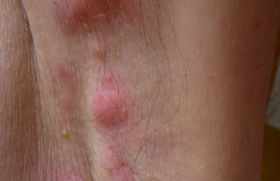
Le lupus érythémateux (LE) est une maladie auto-immune chronique aux manifestations cliniques très variées, allant du LE cutané (LEC) au LE systémique (LES). Aussi, le LEC peut être isolé ou faire partie des manifestations cliniques du LES. Il est traditionnellement pris en charge par différents médicaments immunosuppresseurs posant des problématiques de tolérance et d’échappement, qui pourraient être évitées avec des thérapies ciblées, plus sûres, spécifiques et efficaces. L’arrivée sur le marché de ces dernières pourrait progressivement bouleverser la prise en charge.
Actuellement, plus de 45 molécules font l’objet d’environ 600 études cliniques dans le lupus.
Parmi les molécules pour lesquelles des données existent spécifiquement concernant l’atteinte cutanée figurent le litifilimab, un anticorps monoclonal ciblant le récepteur de surface des cellules dendritiques BDCA2, connu pour réguler la production d'interféron I(1), ainsi que le filgotinib et le lanraplenib, deux inhibiteurs de la voie JAK-STAT qui régulent l’expression de nombreux gènes associés aux processus auto-immuns inflammatoires(2).
Les approches développées plus largement dans le LES se répartissent schématiquement entre trois principes. L’approche cellulaire est l’une des premières à avoir été explorée et vise à supprimer ou à inhiber les cellules B, les cellules T, ou les cellules dendritiques plasma-cytoïdes impliquées dans le processus physiopathologique.
Les cellules B sont non seulement capables de produire des auto-anticorps après leur différenciation en plasmocytes, mais elles présentent également des auto-antigènes aux cellules T et sécrètent des cytokines. Elles ont donc constitué l’une des premières voies visant à développer des thérapies ciblées dans le LES. Le premier médicament mis sur le marché en ce sens est le bélimumab, un Ac monoclonal humanisé ciblant BlyS, le facteur de croissance des lymphocytes B.
Dans la foulée, d’autres cibles impliquées dans l’activation ou la survie des cellules B ont été et sont explorées :
les antigènes de surface des cellules B ; parmi eux, l’obexelimab est un anticorps monoclonal humanisé ciblant CD19, un marqueur de surface des cellules B dont l’inhibition pourrait favoriser la déplétion en cellules B autoréactives et en plasmocytes chez les patients atteints de LES ;
les facteurs de survie des cellules B ; outre le bélimumab, on peut citer le blisibimod, pour lequel les données de phase 3 acquises chez plus de 4 000 patients ayant un LES montrent une efficacité importante, notamment chez les patients ayant une maladie très active, traités par de fortes doses de corticoïdes(3) ;
les fonctions intracellulaires des cellules B (ibrutinib, fénébrutinib, inhibiteurs du protéasome).
L’approche cytokinique est classiquement explorée, car les IFN de type 1 sont impliquées dans la voie inflammatoire associée au lupus, avec un taux qui est associé à l’activité et à la sévérité de la maladie. Actuellement, des études sont conduites avec le sifalimumab, un anticorps monoclonal entièrement humain spécifique de l’IFN-α, en neutralisant la majorité des sous-types d’IFN-α, et l’anifrolumab, un anticorps monoclonal anti-récepteur de l’IFN, qui bloque l’activité des interférons de type 1 comme l’IFN-α et –β. D’autres pistes sont étudiées qui impliquent les cytokines IL-12 ou IL-23.
Finalement, des approches visant à inhiber sélectivement des voies biochimiques intracellulaires, comme celle de la calcineurine, de la voie mTOR ou des JAK-STAT, sont explorées. L’une des difficultés du LES est pour l’heure d’avoir un traitement curatif qui permettrait de contrôler la maladie et d’éliminer simultanément les cellules produisant les auto-anticorps, afin de favoriser une réinduction de la tolérance immunitaire et d’envisager une rémission de la maladie sans traitement. En ce sens, les résultats des premières études sur les cellules T à récepteur antigénique chimérique (CAR-T cells) modifiées pour reconnaître CD19 et d’autres antigènes de surface des cellules B sont aussi à l’étude pour prendre en charge le LES ne répondant pas aux premières lignes de traitement(4). Les premières données montrent une rémission rapide de la maladie, associée à la disparition des autoAc dsDNA, ce qui suggère que les cellules exprimant CD19 pourraient constituer la principale source à l’origine de ces auto-anticorps. Or, une déplétion des cellules B CD19+ et des plasmablastes dans les tissus pourrait aider à la réinitialisation immunitaire et favoriser l’arrêt du traitement immuno-suppresseur. D’autres approches comme le saratimlimab (Ac anti- CD38) sont également à l’étude en ce sens.
D’après la communication «New treatments for cutaneous and systemic lupus erythematosus» de Mirjana Gajic-Veljic (Belgrade, Serbie), EADV 2022
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :