Publié le 25 sep 2023Lecture 3 min
Efficacité du sécukinumab dans la maladie de Verneuil - Résultats de 2 essais contrôlés, randomisés contre placebo de phase III
François CHASSET, service de dermatologie et allergologie, hôpital Tenon, Paris
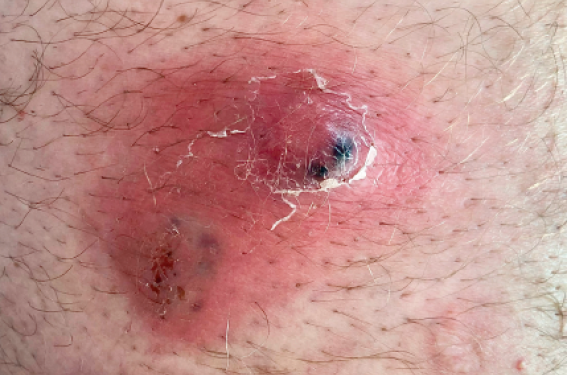
L’hidradénite suppurée (HS) est une maladie inflammatoire chronique fréquente puisqu’elle touche jusqu’à 1 % de la population selon les études, avec un âge de 22 ans en moyenne au début de la maladie. Elle se caractérise dans sa forme classique par des nodules inflammatoires et des abcès profonds, douloureux touchant particulièrement les plis axillaires, inguinaux et les fesses. Les abcès nécessitent souvent une prise en charge chirurgicale et sont très douloureux.
Cette pathologie est associée à un retentissement majeur sur la qualité de vie et s’associe à des troubles de l’humeur et à une anxiété majeure. Le traitement de l’HS est mal codifié. Les antibiotiques sont utilisés pour les poussées et en prévention des récidives en particulier la doxycycline, l’association rifampicine + Dalacine ou le cotrimoxazole avec une efficacité limitée. L’adalimumab a montré son efficacité dans 2 essais contrôlés randomisés de phase III mais a très longtemps été non remboursé. Les cytokines IL17 en particulier IL-17A et IL-17F jouent un rôle important dans la physiopathologie de l’HS. Nous vous avions, il y a quelques mois, rapporté les données de phase II du bimékizumab. Nous rapportons ici les résultats de deux études de phase III contre placebo.
Il s’agissait de deux études cliniques internationales de phase III menées en double aveugle incluant des patients de 18 ans ou plus et ayant une HS modérée à sévère (entre 5 et 20 lésions inflammatoires ou plus affectant au moins deux zones anatomiques distinctes) depuis au moins un an. Ils pouvaient avoir reçu des antibiotiques ou un anti-TNF antérieurement. Les patients étaient randomisés 1:1:1 pour recevoir du sécukinumab 300 mg toutes les 2 semaines, sécukinumab 300 mg toutes les 4 semaines ou un placebo. Après 16 semaines de traitement, les patients sous placebo étaient randomisés dans l’un des groupes sécukinumab avec un traitement poursuivi jusqu’à la semaine 52. Le critère de jugement principal était la diminution d’au moins 50 % du nombre d’abcès et de nodules inflammatoires par rapport à l’inclusion. L’évolution de la douleur et la qualité de vie ont également été analysés.
Au total, l’étude SUNSHINE a inclus 541 patients (56 % de femmes, avec un âge moyen de 36,1 ans) tandis que SUNRISE a inclus 543 patients (56 % de femmes, âge moyen 36,3 ans). La proportion de stade de Hurley variait un peu entre les études mais globalement entre 50-70 % de Hurley II et 30-50 % de Hurley III. Globalement, 80 % des patients avaient déjà reçu des antibiotiques systémiques et 25 % une biothérapie. En ce qui concerne le critère de jugement principal : dans l’étude SUNSHINE, la réponse clinique à 16 semaines était de 45 % dans le groupe sécukinumab toutes les 2 semaines, contre 34 % de ceux sous placebo (OR 1,8 [IC 95 : 1,1-2,7] p = 0,0070) et était à la limite de significativité pour le groupe traité toutes les 4 semaines (42 % vs 34 %, OR = 1,5 [IC 95 : 1,0-2,3 ; p = 0,042). Dans l’étude SUNRISE, la réponse clinique était significativement supérieure dans les deux groupes sécukinumab avec respectivement 42 % et 46 % contre 31 % sous placebo (p = 0,015 et p = 0,0022). Il existait une amélioration significative de la douleur pour la dose à tous les 15 jours et de la qualité de vie pour les deux doses.
Sur le plan de la tolérance, 82 à 86 % des participants sous sécukinumab ont présenté au moins un événement indésirable sans nouveau signal. À noter une candidose œsophagienne sous traitement. À noter également que deux décès sont survenus durant ces deux études, qui n’ont pas été associés au traitement. Enfin, 3 patients ont développé une maladie inflammatoire chronique de l’intestin tous dans l’étude SUNRISE.
En conclusion, cette étude démontre l’efficacité du sécukinumab dans l’HS et a récemment permis son AMM. Il semble licite de ne pas l’utiliser chez des patients avec une maladie de Crohn ou une rectocolite hémorragique, et il faudra surveiller l’apparition de signes digestifs dans cette population, mais ce traitement semble définitivement une avancée importante pour les patients.
Nodules érythémateux dans le cas d’une hidradénite suppurée.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :